据报道,我国拥有完全自主产权的氢氧燃料电池车已在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关该电池的叙述不正确的是( )
| A.正极反应式为:O2+2H2O+4e-===4OH- |
| B.工作一段时间后,电解液中KOH的物质的量不变 |
| C.该燃料电池的总反应方程式为:2H2+O2===2H2O |
| D.该电池工作时每消耗1 mol O2,有2 mol电子转移 |
配制100mL 1mol/L NaCl溶液,下列操作中错误的是()
| A.在托盘天平上放两片大小一样的纸,然后将氯化钠放在纸片上称量 |
| B.把称得的氯化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液移入容量瓶 中 |
| C.用蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液也移入容量瓶中 |
| D.沿玻璃棒往容量瓶中加入蒸馏水,直至溶液凹液面恰好与刻度线相切 |
在100mL某混合溶液中,c(HNO3)=0.4mol/L,c(H2SO4)=0.1mol/L,向其中加入 1.92g铜粉,微热,充分反应后溶液中c(Cu2+)为()
| A.0.15mol/L | B.0.3mol/L |
| C.0.225mol/L | D.无法计算 |
某有机物与过量的金属钠反应,得到VA升气体,另一份等质量的该有机物与小苏打反应得到气体VB升(同温、同压),若VA>VB(VB≠0),则该有机物可能是()
| A.HOCH2CH2OH | B.CH3COOH |
| C.HOOC-COOH | D.HOOC-C6H4-OH |
经一定时间后,可逆反应aA+bB  cC中物质的含量A%和C%随温度的变化曲线如右图所示。下列说法正确的是()
cC中物质的含量A%和C%随温度的变化曲线如右图所示。下列说法正确的是()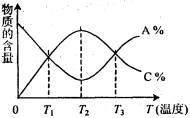
| A.该反应在T1、T3温度时达到化学平衡 |
| B.该反应在T2温度时达到化学平衡 |
| C.该反应的逆反应是放热反应 |
| D.升高温度,平衡会向正反应方向移动 |
mA(g)+nB(g) pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图2-32中实线所示,有关叙述正确的是()
pC(g)(正反应为放热反应)的可逆反应,在恒温条件下,平衡时B在混合物中的含量(B%)与压强的关系如图2-32中实线所示,有关叙述正确的是()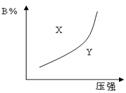
| A.m+n> p |
| B.x点的速率关系为v正>v逆 |
| C.n>p |
| D.x点比y点混合物反应速率快 |