对于Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g)的化学反应(反应放热),下列叙述一定正确的是( )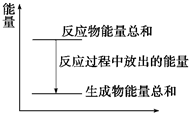
| A.反应过程中的能量关系可用上图表示 |
| B.1 mol锌的能量高于1 mol H2所含的能量 |
| C.若将该反应设计成原电池,锌为负极 |
| D.若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L |
在相同温度时,100 mL 0.01 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是( )
| A.中和时所需NaOH的量 |
| B.电离度 |
| C.H+的物质的量 |
| D.CH3COOH的物质的量 |
用0.01 mol·L-1NaOH溶液完全中和pH=3的下列溶液各100 mL,需NaOH溶液体积最大的是( )
| A.盐酸 | B.硫酸 | C.高氯酸 | D.醋酸 |
已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
| A.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l)ΔH="-4b" kJ·mol-1 |
| B.C2H2(g)+5[]2O2(g)====2CO2(g)+H2O(l)ΔH="2b" kJ·mol-1 |
| C.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l)ΔH="-2b" kJ·mol-1 |
| D.2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l)ΔH="b" kJ·mol-1 |
已知NaH2PO4溶液呈酸性,在水溶液中存在如下水解平衡:H2PO-4+H2O H3PO4+OH-,现将0.1 mol·L-1NaH2PO4溶液稀释后,增大的是( )
H3PO4+OH-,现将0.1 mol·L-1NaH2PO4溶液稀释后,增大的是( )
| A.[H+] | B.[OH-] | C.[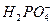 ] ] |
D.KW |
mA(s)+nB(g) pC(g)的可逆反应,在室温条件下φ(B)与压强(p)的关系如图4所示,则下列有关叙述正确的是( )
pC(g)的可逆反应,在室温条件下φ(B)与压强(p)的关系如图4所示,则下列有关叙述正确的是( )
图4
A.m+n<p
B.n>p
C.X点时混合物的正反应速率大于逆反应速率
D.X点比Y点混合物的反应速率慢