(4分)请用方程式写出过氧化钠应用于呼吸面具的原理:
_______________________________________________________
五种短周期元素的性质或原子结构信息如下表:
| 元素 |
元素性质或原子结构信息 |
| Q |
原子核外有6种不同运动状态的电子 |
| R |
最外层电子数是次外层电子数的3倍 |
| X |
气态氢化物的水溶液呈弱碱性 |
| Y |
第三周期元素的简单离子中离子半径最小 |
| Z |
单质为银白色固体,在空气中燃烧发出黄色火焰 |
请根据表中信息回答下列问题:
(1)Q原子的电子排布式为___________________________,其同位素有。
(2)R与Z组成的化合物的化学式是。
(3)X气态氢化物分子的空间构型为。X的最高价氧化物对应的水化物其浓溶液与同类物质相比在化学性质上表现的特殊性有。
(4)Y单质与V2O5反应的化学方程式为。
(5)在1.01×105Pa、298K时,1.4gQR气体在1.6gR2气体中完全燃烧,生成QR2气体时放出14.15kJ热量,表示QR燃烧的热化学方程式为。
氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂和生产含氟牙膏等。实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵:
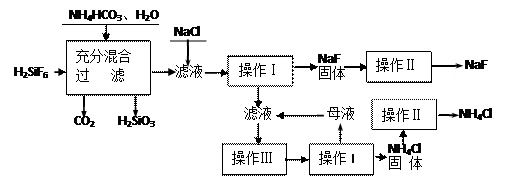 |
有关物质在水中溶解度(g/100gH2O)如下:
| 温度 |
10℃ |
20℃ |
30℃ |
溶解度:20℃NaF—4 0℃NH4F—100; 常温Na2SiF6微溶于水 |
| NH4Cl溶解度 |
33.3 |
37.2 |
41.4 |
请回答下列问题:
(1)操作Ⅰ需要用到的玻璃仪器有 。
(2)上述流程中发生两步反应,化学方程式为 ,
。
(3)操作II的作用是 ,
操作Ⅲ的具体过程是 。
(4)流程中NH4HCO3必须过量,其原因是
_______________________________________________________________________。
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
|
||||
 |
||||

| 实验序号 |
实验操作 |
现象 |
结论 |
| Ⅰ |
将氯水滴入品红溶液 |
溶液褪色 |
氯气与水反应的产物有漂白性 |
| Ⅱ |
氯水中加入 NaHCO3粉末 |
有无色气泡产生 |
氯气与水反应的产物具有较强的酸性 |
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由。
。
②请利用上述装置设计一个简单的实验,验证Cl-和Br-的还原性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2
并进行有关实验。
①B中发生反应的化学方程式为 。
② 欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁的操作是 。
③ 试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,则所得溶液中溶质的物质的量浓度是 (气体按标准状况计算)。
已知LiH、NaH及LiAlH4都是常见的金属的氢化物,其中LiAlH4可由下列途径合成:4LiH + AlCl3  LiAlH4+ 3LiCl。
LiAlH4+ 3LiCl。
试探究下列相关问题
(1)下列有关说法正确的是▲。
A.该反应是氧化还原反应
B.乙醚(C2H5OC2H5)是非极性分子
C.化学性质锂与镁相似,铝与铍相似
D.LiAlH4具有还原性
(2)正在载入...
镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力,其中铜钙合金的晶胞结构为: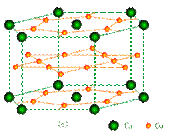
试回答下列问题
①在周期表中Ca处于周期表▲区。
②铜原子的基态核外电子排布式为:▲。
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n= ▲(填数值);氢在合金中的密度为:▲。
(3)中美科学家合作发现钙和锶在C60上吸附很强,可以均匀地覆盖在C60表面上,形成M32C60。非常适于实际应用。 Ca32C60上可吸附至少92个氢分子(如图)。
有关说法正确的是▲。
A.钙的第一电离能和电负性均比锶的第一电离能小
B.C60中碳原子杂化方式为sp3
C.Ca32C60储氢是与H2发生加成反应
D.吸附相同数目氢分子时,储氢质量分数(wt%。)Ca32C60比Sr32C60高
盐酸西替利嗪在临床上广泛用于呼吸系统、皮肤和眼部过敏性疾病,它的一种合成路线如下: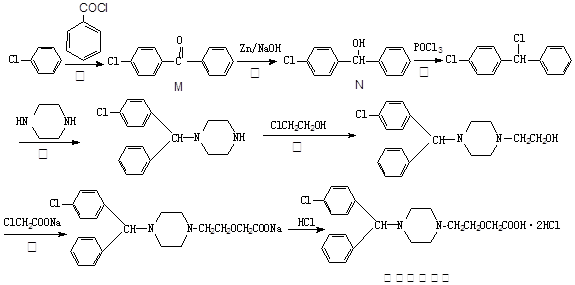 (1)上述反应中,属于取代反应的是 ▲(填序号).
(1)上述反应中,属于取代反应的是 ▲(填序号).
(2)物质M核磁共振氢谱有 ▲个峰。
(3)盐酸西替利嗪中含氧官能团是 ▲(写名称)。
(4)反应④中会产生一种含氮副产物,最有可能是 ▲。
(5)图中物质N符合下列条件的异构体有 ▲种。
①能与氯化铁溶液发生显色反应②含有-CH2Cl③含有联苯(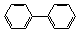 )结构。
)结构。
(6)抗血栓药氯吡格雷的手性合成如下: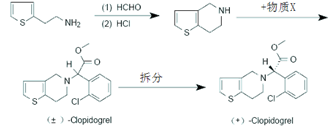
已知X的分子式为:C9H8Cl2O2,则X的结构式为 ▲。氯吡格雷中手性碳原子数目为▲个。
(7)已知: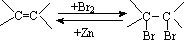
试以中药材大青叶的提取物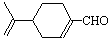 (紫苏醛)和甲醇为原料合成(紫苏
(紫苏醛)和甲醇为原料合成(紫苏
酸甲酯)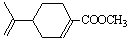 试写出合成路线。合成路线流程图示例如下:
试写出合成路线。合成路线流程图示例如下: