在一定条件下,可逆反应:N2+3H2 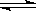 2NH3(正反应放热)达到平衡,当单独改变下列条件后,有关叙述错误的是( )。
2NH3(正反应放热)达到平衡,当单独改变下列条件后,有关叙述错误的是( )。
| A.加催化剂,v正、v逆都发生变化且变化的倍数相等 |
| B.加压,v正、v逆都增大,且v正增大倍数大于v逆增大倍数 |
| C.降温,v正、v逆都减小,且v正减小倍数大于v逆减小倍数 |
| D.加入氩气,v正、v逆都增大,且v正增大倍数大于v逆增大倍数 |
下列关于化学的叙述中,错误的是
| A.在化工生产中应遵循“绿色化学”的思想 |
| B.通常用来衡量一个国家的石油化学工业发展水平的标志是乙烯的产量 |
| C.在元素周期表的金属和非金属分界线附近寻找半导体材料 |
| D.根据元素周期律,由HClO4可以类推出氟元素也存在最高价氧化物的水化物HFO4 |
已知A2-核内有x个中子,A原子的质量数为m,则n g A2-所含电子的总物质的量是
A. mol mol |
B. mol mol |
C.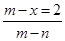 mol mol |
D.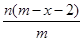 mol mol |
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,电池放电时时的反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,下列对电池放电时的分析正确的
| A.Pb为正极被氧化 | B.电子从PbO2 流向外电路 |
| C.SO42-向PbO2处移动 | D.电解质溶液pH不断增大 |
下列反应的离子方程式正确的是
| A.钠与水的反应:Na+H2O=Na++OH-+H2↑ |
| B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| C.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
| D.氢氧化铝中和胃酸:Al(OH)3+3H+=Al3++3H2O |
铁镍蓄电池又称爱迪生电池,放电时的总反应为Fe+Ni2O3+3H2O==Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,负极为Fe |
| B.电池放电过程中,负极附近溶液的pH降低 |
| C.电池放电时,若外电路中有2mol电子转移,则内电路中有2molOH-移向正极 |
| D.电池放电时,负极反应为Fe+2OH--2e-==Fe(OH)2 |