工业上将氨气和空气的混合气体通过铂铑合金网发生氨氧化反应,若有标准状况下 VL 氨气完全反应,并转移 n 个电子,则阿伏加德罗常数(NA)可表示为:
| A. 11.2n/5V | B. 5V/11.2n | C. 22.4V/5n | D. 22.4n/5v |
.在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子可能是
| A.Mg2+、Al3+、Fe3+ | B.H+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ | D.Na+、Mg2+、Al3+ |
CO2通入下列各溶液中,不可能产生沉淀的是
| A.氯化钙溶液 | B.饱和碳酸钠溶液 | C.硅酸钠溶液 | D.澄清石灰 |
将18mL充满NO和NO2混合气体的试管倒立于水中,过一会儿,当试管内有4mL水上升时,液面不再变化. 原混合气体中NO和NO2的体积比为(在相同条件下)
A.1:1. B2:1 C.7:2 D.2:7
用NA表示阿伏德罗常数,下列叙述正确的是
| A.标准状况下,22.4LH2O含有的分子数为1 NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C.通常状况下, NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl-个数为 NA |
工业上用洗净的废铜屑作原料来制备硝酸铜,为节约原料和防止环境污染,宜采用的方法是
A.Cu+HNO3(稀) Cu(NO3)2 Cu(NO3)2 |
B.Cu+HNO3(浓) Cu(NO3)2 Cu(NO3)2 |
C.Cu CuSO4 CuSO4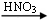 Cu(NO3)2 Cu(NO3)2 |
D.Cu CuO CuO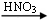 Cu(NO3)2 Cu(NO3)2 |