在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g)  2c(g) △H1<0; x(g)+3y(g)
2c(g) △H1<0; x(g)+3y(g)  2z (g) △H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是:
2z (g) △H2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是:
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。SnSO4的实验室制备设计路线如下: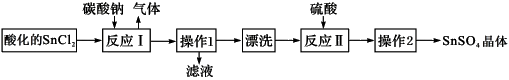
下列有关说法正确的是
| A.SnCl2酸化是为了防止溶解时发生水解 |
| B.反应I中发生的离子反应为:CO32-+2H+=CO2↑+ H2O |
| C.漂洗时,将固体置于烧杯中,加蒸馏水洗涤过滤2-3次 |
| D.操作1为过滤,操作2为盐析 |
光谱研究表明,易溶于水的SO2所形成的溶液中存在着下列平衡: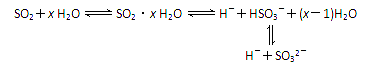
据此,下列判断中正确的是
| A.该溶液中存在着SO2分子 |
| B.该溶液中H+浓度是SO32-浓度的2倍 |
| C.向该溶液中加入足量的酸SO2气体都能放出 |
| D.向该溶液中加入NaOH可得到Na2SO3、NaHSO3和NaOH的混合溶液 |
向等物质的量浓度的MgSO4和NaHSO4的混合溶液中逐滴滴入一定量的Ba(OH)2溶液,下列离子方程式与事实不相符的是
| A.H++SO42-+Ba2++OH-→ BaSO4↓+H2O |
| B.2H++SO42-+Ba2++2OH-→BaSO4↓+2H2O |
| C.Mg2++H++2SO42-+2Ba2++3OH-→Mg(OH)2↓+2BaSO4↓+H2O |
| D.Mg2++2H++2SO42-+2Ba2++4OH-→Mg(OH)2↓+2BaSO4↓+2H2O |
下列离子方程式正确的是
| A.已知电离平衡常数:H2CO3>HClO>HCO3—,向NaClO溶液中通入少量CO2:2ClO—+CO2+H2O=2HClO+CO32— |
| B.向硫酸氢钠溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++ OH-=BaSO4↓+ H2O |
| C.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++ 2I-=2Fe2++ I2 |
D.硫氢根离子的电离方程式:HS-+H2O H3O++S2- H3O++S2- |
仅用下表提供的仪器(夹持仪器和试剂任选),不能实现相应实验目的的是
| 选项 |
实验目的 |
仪器 |
| A |
从食盐水中获得NaCl晶体 |
蒸发皿、玻璃棒、酒精灯 |
| B |
用稀H2SO4、Na2CO3溶液比较元素S与C的非金属性强弱 |
试管、胶头滴管 |
| C |
用8.0mol·L-1的盐酸配制250mL1.5mol·L-1的盐酸 |
250mL容量瓶、玻璃棒、烧杯 |
| D |
测定NaOH溶液的物质的量浓度 |
酸(碱)式滴定管、胶头滴管、锥形瓶、烧杯 |