右图所示是一种新近开发的固体氧化物燃料电池。它以掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体为固体电解质,在熔融状态下传导氧离子 (O2-),其中多孔电极a、b均不参与电极反应。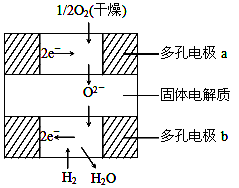
下列判断不正确的是( )
| A.采用多孔电极的目的是易于吸附气体 |
| B.有H2放电的b极为电池的负极 |
| C.a极对应的电极反应为O2+2H2O+4e-=4OH- |
| D.b极对应的电极反应为2H2-4e-+2O2-=2H2O |
设NA代表阿伏加德罗常数,下列叙述正确的是()
| A.标准状况下,11.2L的O2和NO的混合物含有的分子数约为0.5×6.02×1023 |
| B.1mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA |
| C.常温常压下42g 乙烯和丁烯混合气体中,碳氢键的数目为6NA |
| D.6.4g SO2与3.2g氧气反应生成SO3,转移电子数为0.2NA |
t℃时,水的离子积为KW。在该温度下,混合可溶性的一元酸HA和一元碱BOH的溶液,下列有关混合液的各种关系中,可确认混合液呈中性的是 ()
| A.pH=7 | B.c(OH-)=c(H+)=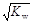 |
| C.c(A-) > c(B+) | D.c(H+)-c(OH-)=c(A-)-c(B+) |
下列各溶液中,一定能大量共存的是()
| A.Fe2+、Na+、SO42-、H2O2 | B.SO32-、MnO4-、H+、K+ |
| C.Pb2+、K+、SO42-、Cl- | D.Na+、SO32- 、K+、SO42- |
随着从们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是()
| A.无水硫酸铜、蔗糖 | B.生石灰、硫酸亚铁 |
| C.食盐、硫酸亚铁 | D.生石灰、食盐 |
在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图7表示200℃时容器中A、B、C物质的量随时间的变化关系,图8表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g),图7表示200℃时容器中A、B、C物质的量随时间的变化关系,图8表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol•L-1•min-1
B.图8所知反应xA(g)+yB(g) zC(g)的ΔH>0,且a=2
zC(g)的ΔH>0,且a=2
C.若在图7所示的平衡状态下,再向体系中充入He,此时v正>v逆
D.200℃时,向容器中充入1.6molA和0.8molB,达到平衡时,A的转化率大于50%