一定条件下,通过下列反应可实现燃煤烟气中硫的回收: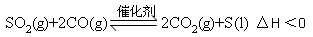
若反应在恒容的密闭容器中进行,下列有关说法正确的是
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其它条件不变,分享出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其它条件不变,使用不同催化剂,该反应的平衡常数不变 |
已知反应X+Y= M+N为吸热反应,对这个反应的下列说法中正确的是()
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.X和Y的总能量一定低于M和N的总能量 |
已知乙酸和乙酸乙酯的混合物中氢元素的质量分数为7%,则混合物中碳元素的质量分数为 ( )
| A.42% | B.44% | C.48.6 % | D.91.6% |
下列排列顺序正确的是()
①热稳定性:H2O>HF>H2S②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4 ④沸点:癸烷>异戊烷>丙烷
| A.①③ | B.②③ | C.①④ | D.②④ |
下列说法正确的是()
| A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
| B.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
| C.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源 |
| D.凡含有食品添加剂的食物对人体健康均有害,不宜食用 |
设NA为阿伏加德罗常数,下列叙述中正确的是 ( )
| A.常温下11.2 L的甲烷气体含有甲烷分子数为0.5NA个 |
| B.14 g乙烯和丙烯的混合物中总原子数为3NA个 |
| C.0.1 mol/L的氢氧化钠溶液中含钠离子数为0.1NA个 |
| D.18 g D2O中含有质子数为10NA个 |