在标准状况下,44.8L的NH3气体质量为 g, 其中含 个氢原子,其中含 molN;将其溶于水配成200mL的溶液,其物质的量浓度为 _ mol/L。
等物质的量的CH4和NH3两种气体中, H原子数之比为 ,二者的质量之比为 ,在同温同压下的体积之比为 。
(10分)塑化剂是工业上被广泛使用的高分子材料助剂,在塑料加工中添加这种物质,可以使其柔韧性增强,容易加工。塑化剂可合法用于工业生产,但禁止作为食品添加剂。截止2011年6月8日,台湾被检测出含塑化剂食品已达961种,据媒体报道,2012年岁末,我国大陆多种著名品牌白酒也陷入了塑化剂风波。
常见塑化剂为邻苯二甲酸酯类物质,某有机物J(C19H20O4)是一种塑料工业中常用的塑化剂,可用下列合成路线合成。
已知:Ⅰ.
Ⅱ.控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应;
Ⅲ.F与浓溴水混合不产生白色沉淀。
请回答下列问题:
(1) F中官能团的电子式为________。
(2)写出反应①④的化学反应方程式:
反应①________________________________。反应④________________________________。
(3)C4H10O的同分异构体中属于醇类的有多种,写出其中具有手性碳原子的同分异构体的结构简式:________________。
(4)以含碳原子数不同的苯的同系物为原料,可以合成不同种类的塑化剂。教材中苯及其同系物的通式是CnH2n-6(n≥6),某同学根据等差数列公式推导出该系列的通式却是Cn+5H2n+4,老师告诉该同学他推导出的通式也是正确的,但其中n的意义和取值范围与教材中的通式不同,请问:通式Cn+5H2n+4中n的意义是________。
(10分)2014年4月,英国《每日邮报》报道制造太阳镜、婴儿奶瓶、太空杯和光盘的主要材料都是聚碳酸酯,聚碳酸酯在一定条件下可释放出有毒的双酚A( )。聚碳酸酯不耐高温,100 ℃时释放出的双酚A是25 ℃时的50倍。双酚A进入人体后,会溶解在身体的血管里,导致致命性的血管疾病。请回答下列问题:
)。聚碳酸酯不耐高温,100 ℃时释放出的双酚A是25 ℃时的50倍。双酚A进入人体后,会溶解在身体的血管里,导致致命性的血管疾病。请回答下列问题:
Ⅰ.下列关于双酚A的说法不正确的是________(填序号)
A.利用聚碳酸酯制成的茶杯来泡茶时对人体无害
B.双酚A的分子式是C15H16O2
C.双酚A的核磁共振氢谱显示有4组峰,且峰面积之比为1∶2∶2∶3
D.1 mol双酚A最多消耗2 mol Br2
Ⅱ.聚碳酸酯(简称PC)是分子链中含有碳酸酯基的高分子聚合物,其合成流程如下:
(1)反应①②③④⑤中属于取代反应的有________。
(2)CH3CH==CH2与Cl2加成产物的同分异构体有________种(不含加成产物)。
(3)写出反应⑤⑦的化学方程式:
反应⑤________________________。反应⑦________________________。
(8分)下列是八种环状的烃类物质:
(1)金刚烷的一氯取代产物有________种,立方烷的二氯取代产物有________种。
(2)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):______________________、______________________。
(3)以立方烷的一种属于芳香烃的同分异构体为起始物质,通过一系列反应可制得苯乙炔,写出有关化学方程式(所需的试剂自选): ____________________________。
(4分) 甲、乙、丙、丁四种烃的含氧衍生物,其分子中都含有一个或一个以上的官能团,通过下列转化关系可由甲制取丁:
若丁的相对分子质量总为甲的两倍,乙的相对分子质量总大于丙。回答下列问题:
(1)乙的分子结构中一定含有的官能团是(填名称);丙的分子结构中一定含有的官能团的电子式为。
(2)乙、丙的相对分子质量之差为(填一个数字)的整数倍。
(3)满足上述转化关系的甲、乙、丙、丁中,相对分子质量最小的甲的结构简式为。
吲哚昔酚 (idoxifene)可用于治疗骨质疏松症,它的合成路线如图。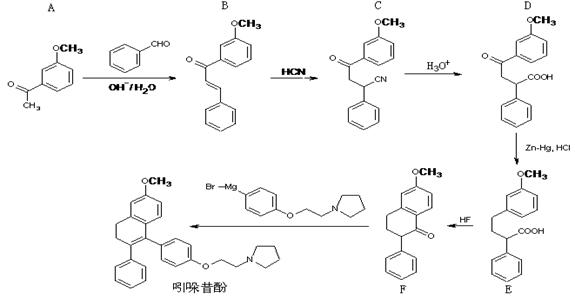
(1)化合物A的分子式是,1molA最多能与H2发生反应
(2)反应类型:B→C; D→E
(3)D中含氧官能团有:(写名称)。
(4)化合物E能发生的反应类型是(填入序号)
| A.加成反应 | B.酯化反应 | C.水解反应 | D.加聚反应 |
(5)E→F中还有一种副产物G生成,G与F互为同分异构体,且含有三个六元环,G 结构简式为:。
(6)满足下列四个条件的A的同分异构体数目有种。
①苯的衍生物,且苯环上只有两个互为对位的取代基;②能发生银镜反应;③与FeCl3溶液作用不显色;④不与氢氧化钠水溶液反应
(7)2,2-二甲基戊酸[CH3CH2CH2C(CH3)2COOH]是有机合成中间体,请设计合理的方案以丙酮(CH3COCH3)为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,注明反应条件)
提示:①合成过程中无机试剂任选;②丙酮分子间能发生上图合成路线中A→B的类似反应;
③合成路线流程图示例:CH3CH2OH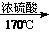 CH2=CH2
CH2=CH2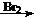 CH2Br-CH2Br
CH2Br-CH2Br