应用元素周期律的有关知识,可以预测我们不知道的一些元素及其化合物的性质。下列预测中不正确的是( )
①Be的氧化物的水化物可能具有两性②Tl能与盐酸和NaOH溶液作用均产生氢气③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱⑤SrSO4是难溶于水的白色固体⑥H2Se是无色,有毒,比H2S稳定的气体
| A.①②③④ | B.②④⑥ | C.①③⑥ | D.②④⑤ |
下列物质中既不能发生水解反应也不能发生还原反应的是()
| A.葡萄糖 | B.纤维素 | C.乙醇 | D.蔗糖 |
将1.62g淀粉在一定条件下水解,反应一段时间后,向容器中加入足量的银氨溶液,结果析出0.108g银,则淀粉的水解率为 ( )
| A. 8% | B. 10% | C. 5% | D.无法计算 |
具有一个醇羟基的有机物A与8g乙酸充分反应生成了10.2g乙酸乙酯,经分析还有2g乙酸剩余,下列醇中有可能是A的是()
A.C2H5OH B.C6H5—CH2—OH
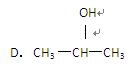
下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是()
| A.金属钠 | B.溴水 | C.碳酸钠溶液 | D.紫色石蕊溶液 |
当乙酸分子中的O都是18O,乙醇分子中的O都是16O,二者在一定条件下反应所生成物中的水的相对分子质量为()
| A.16 | B.18 | C.20 | D.22 |