.以硫酸铜溶液作电解液,对含有杂质Fe、Zn、Ag的粗铜进行电解精炼。下列叙述正确的是( )
①粗铜与直流电源负极相连
②阴极发生的反应为Cu2++2e-=Cu
③电路中每通过3.0l×1023个电子,得到的精铜质量为16g
④杂质Ag以Ag2SO4的形式沉人电解槽形成“阳极泥”
| A.②③ | B.②④ | C.③④ | D.①③ |
一定条件下,将NO2与SO2以2∶3的体积比置于密闭容器中发生上反应:NO2(g)+SO2(g) SO3(g)+NO(g),测得上述反应平衡时NO2与SO2体积比为1∶4,则平衡时SO2(g)的转化率是()
SO3(g)+NO(g),测得上述反应平衡时NO2与SO2体积比为1∶4,则平衡时SO2(g)的转化率是()
| A.5/6 | B.3/4 | C.5/9 | D.2/3 |
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元
素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是()
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y> W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
下列判断正确的是()
| A.元素周期表中查得的相对原子质量为同位素的相对原子质量 |
| B.化学键的变化一定会引起化学反应的变化 |
| C.只含有共价键的物质一定是共价化合物 |
| D.全部由极性键构成的分子不一定是极性分子 |
已知某可逆反应在密闭容器中进行:A(g)+2B(g)  3C(g)+D(s) △H<0,下图中曲线a 代表一定条件下该反应的过程,若使a曲线变为b曲线,可采用的措施是()
3C(g)+D(s) △H<0,下图中曲线a 代表一定条件下该反应的过程,若使a曲线变为b曲线,可采用的措施是()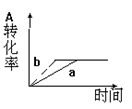
| A.增大A的浓度 | B.增大容器的体积 |
| C.加入催化剂 | D.升高温度 |
已知:2M(g) N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是()
| A.a、b、c、d四个点中处于平衡状态的点是a、b |
| B.反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C.若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D.若40min后出现如图所示变化,则可能是加入了某种催化剂 |