氰化物有剧毒,我国工业废水中氰化物(CN-)的最高允许排放浓度为0.5 mg/L;对废水中CN-的处理方法是:在碱性条件下,用Cl2将废水的中CN-转化成N2和CO2等,使废水得到净化。发生的反应为:2CN-+ 8OH-+ 5Cl2 = 2CO2 ↑+ N2 ↑+10 Cl-+ 4H2O ;下列有关说法正确的是( )
| A.上述反应中氧化产物只有N2 |
| B.经测定,NaCN的水溶液呈碱性,说明CN—能促进水的电离 |
| C.若上述反应生成0.4 mol CO2,则溶液中阴离子增加的物质的量为2 mol |
| D.现取1 L含CN-1.04mg/L的废水,至少需用4.0×10-5mol Cl2处理后才符合排放标准 |
下列化学用语不能正确解释相关事实的是
| A.碱性氢氧燃料电池的正极反应:H2 - 2e- + 2OH-="==" 2H2O |
B.用电子式表示NaCl的形成过程: |
| C.向含有Hg2+的废水中加入Na2S可除去Hg2+:Hg2+ + S2- ="==" HgS↓ |
D.汽车尾气系统的催化转化器可降低NO等的排放:2CO+ 2NO 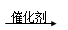 2CO2 +N2 2CO2 +N2 |
下列各组物质状态发生变化时,所克服的微粒间作用力完全相同的是
| A.碘的升华和干冰气化 | B.二氧化硅和干冰熔化 |
| C.苯和硝酸钾熔化 | D.食盐的熔化和冰的融化 |
下列有关化学键与晶体结构说法正确的是
| A.两种元素组成的分子中一定只有极性键 |
| B.离子化合物的熔点一定比共价化合物的高 |
| C.非金属元素组成的化合物一定是共价化合物 |
| D.含有阴离子的化合物一定含有阳离子 |
下列有关物质的性质或应用的说法正确的是
| A.煤的干馏和石油的分馏均属化学变化 | B.聚乙烯的结构简式为CH2===CH2 |
| C.盐析可提纯蛋白质并保持其生理活性 | D.石油分馏可获得乙烯、丙烯和丁二烯 |
下列说法正确的是
A.油脂和蛋白质均属于高分子化合物
B.二氧化硅是太阳能电池的主要材料
C.Na、C、S都能直接与氧气反应,生成两种相应的氧化物
D.蔗糖、麦芽糖的分子式都是C11H12O11,二者互为同分异构体