从海水中提取的溴占世界产溴量的1/3。已知溴水呈橙色,将SO2气体通入溴水时,可以观察到溴水褪色。则下列有关叙述中正确的是( )
| A.SO2使溴水褪色,显示了SO2的漂白性 |
| B.SO2是形成酸雨的唯一原因 |
| C.从溴水中提取单质溴,可以用乙醇进行萃取 |
| D.SO2使溴水褪色,显示了SO2的还原性 |
下列气体中,主要成分不是甲烷的是
| A.天然气 | B.水煤气 | C.坑气 | D.沼气 |
对发现元素周期律贡献最大的化学家是
| A.牛顿 | B.道尔顿 | C.阿佛加德罗 | D.门捷列夫 |
下列各装置能构成原电池的是()。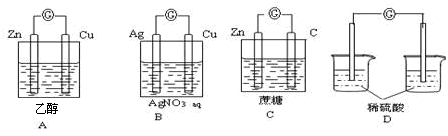
在反应H2 + Cl2= 2HCl中,已知断开1 mol H-H需要能量436 kJ,断开1 mol Cl-Cl需要能量243 kJ,断开1 mol H-Cl需要能量431 kJ,判断该反应是()。
| A.吸热反应 | B.放热反应 | C.放出832 kJ热量 | D.吸收183 kJ热量 |
实验室准备较快地制取氢气,可采用的方法是()。
| A.用纯锌与稀硫酸反应 | B.用纯锌与稀硝酸反应 |
| C.用粗锌与稀硝酸反应 | D.在CuSO4溶液中浸泡过的纯锌与稀硫酸反应。 |