一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)  H2(g)+I2(g)。若c(HI)由0.1 mol/L 降到0.07 mol/L时,需要15 s,那么c(HI)由0.07 mol/L 降到0.05 mol/L时,所需反应的时间为
H2(g)+I2(g)。若c(HI)由0.1 mol/L 降到0.07 mol/L时,需要15 s,那么c(HI)由0.07 mol/L 降到0.05 mol/L时,所需反应的时间为
| A.等于5 s | B.等于10 s | C.大于10 s | D.小于10 s |
下列实验过程中,始终无明显现象的是( )
A. 通入 通入 溶液中 溶液中 |
B. 通入已酸化的 通入已酸化的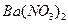 溶液中 溶液中 |
| C.一充满NO2试管倒扣在水中 | D.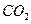 通入 通入 溶液中 溶液中 |
设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A.1.00molSiO2中含有分子数目为1NA |
| B.常温常压下,1 mol臭氧和1 .5mol氧气质量相同 |
| C.标准状况下,2.24L SO3含有分子的数目为0.1NA |
| D.1mol Cl2与足量Fe反应,转移的电子数为3NA |
开发新材料是现代科技发展的方向之一。下列有关材料的说法不正确的是( )
| A.利用碳化硅(俗称硅石)的硬度很大,可用作砂纸的磨料 |
| B.利用高纯硅的半导体性能,可以制成光电池 |
| C.透明陶瓷(如氧化铝)具有良好的光学性能,可制防弹汽车的车窗 |
| D.硅橡胶既耐高温又耐低温,用于制造火箭、导弹、飞机的零件 |
H-是负一价的阴 离子,它可与NH3发生以下反应:H-+NH3= H2+NH2-,下列有关这个反应的说法中正确的是(
离子,它可与NH3发生以下反应:H-+NH3= H2+NH2-,下列有关这个反应的说法中正确的是( )。
)。
| A.它属于置换反应 | B.该反应中H-是还原剂 |
| C.该反应中NH3被氧化 | D.反应中被氧化和被还原的元素都是H元素 |
下列反应的离子方程式书写正确的是( )
| A.饱和石灰水与稀硝酸反应:Ca(OH)2+2H+===Ca2++2H2O |
| B.稀硫酸与锌反应:H2SO4+Zn===Zn2++SO42—+H2↑ |
| C.碳酸钙与稀盐酸反应:CaCO3+2H+===Ca2++CO2↑+H2O |
| D.小苏打溶液与NaOH反应:HCO3—+OH-===H2O+CO32— |