2005年诺贝尔化学奖获得者施罗克等人发现,金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为( )
①2MoS2+7O2 2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O
2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4C1 ④H2MoO4 MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是
| A.反应①和⑤都属于置换反应 |
| B.MoO3属于碱性氧化物 |
| C.在反应①中Mo和S均被氧化 |
| D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为2:2:3 |
【改编】下列说法正确的是
| 选项 |
实验 |
解释或结论 |
| A |
用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色 |
该溶液中一定不含有K+ |
| B |
用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧 |
CO2、H2O与Na2O2反应是放热反应 |
| C |
向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀 |
该溶液中含有SO42- |
| D |
利用一束强光照射明矾溶液,产生光亮的“通路”, |
明矾一定发生了水解 |
【原创】物质A在一定条件下反应制得新型纤维酸类降脂药克利贝特,其结构简式如图所示,下列有关叙述正确的是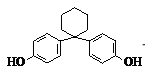
| A.物质A分子中含有2个手性碳原子 |
| B.物质A分子中所有碳原子可能位于同一平面内 |
| C.1 mol物质A最多可以与含4molBr2的溴水反应 |
| D.物质A可以发生加成反应、氧化反应、水解反应 |
下列说法中正确的是
| A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<0则该反应一定能自发进行 |
| B.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 |
| C.催化剂可以加快化学反应速率,也能增大化学反应的焓变 |
| D.NH3•H2O溶液加水稀释后,溶液中c(NH3•H2O)/c(NH4+)的值增大 |
室温下,将1mol的CuSO4•5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2,CuSO4•5H2O受热分解的化学方程式为:CuSO4•5H2O(s)  CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
| A.△H2>△H3 | B.△H1<△H3 | C.△H1+△H3=△H2 | D.△H1+△H2>△H3 |
【改编】短周期元素W、X、Y、Z的原子序数依次增大,W的单质是空气中体积分数最大的气体,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的最外层电子数等于其最内层电子数,X、Y、Z的简单离子的电子层结构相同。下列说法正确的是
| A.气态氢化物的稳定性: Y>X>W |
| B.四种元素的原子中W原子半径最大 |
| C.四种元素中最高价氧化物的水化物酸性Y最强 |
| D.化合物XY2与ZY2分子中的化学键类型相同 |