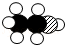
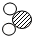
在点燃条件下,M和N反应生成X和Y.反应前后分子变化的微观示意图如下所示(其中“ ”代表氢原子,“
”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).下列叙述中,不正确的是( )
”代表氧原子).下列叙述中,不正确的是( )
| 物质 |
M |
N |
X |
Y |
| 微观示意图 |
 |
 |
 |
 |
A.生成物均为氧化物
B.在该反应中,生成X和Y的质量比为9:22
C.M中碳、氢、氧三种元素的质量比为12:3:8
D.在该反应中,M和N两种物质的分子个数比为1:3
在一定条件下,反应物的溶液中溶质质量分数越大,化学反应速率越快.现有100g溶质质量分数为27%的硫酸溶液与足量的锌粒反应,为了减缓化学反应的速率,而又不影响生成氢气的总质量,可向该溶液中加入适量的( )
| A.水 | B.盐酸溶液 | C.碳酸钠溶液 | D.氢氧化钠溶液 |
下列实验方案中,能达到实验目的是( )
| 选项 |
实验目的 |
实验方案 |
| A |
除去CaO中的CaCO3 |
加足量稀盐酸,过滤 |
| B |
检验一瓶气体是否为二氧化碳 |
将燃着的木条伸入瓶中,观察是否熄灭 |
| C |
除去氯化钠固体中的少量碳酸钠 |
加入适量稀盐酸,充分反应后,蒸发 |
| D |
鉴别氯化钠溶液、氢氧化钠溶液和稀盐酸 |
各取少量溶液于试管中,分别滴加无色酚酞溶液,观察溶液颜色的变化 |
甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )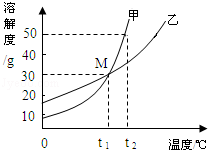
| A.t1℃时,甲、乙各30g分别加入70g水中均恰好完全溶解 |
| B.t1℃时,甲、乙两物质形成的溶液溶质的质量分数相等 |
| C.t2℃时,在l00g水中放入60g甲,所得溶液溶质的质量分数为37.5% |
| D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和 |
铝可与碱溶液发生反应:2Al+2NaOH+2H2O=2NaAlO2+3X↑,关于此反应的叙述不正确的是( )
| A.X的化学式为H2 |
| B.NaAlO2属于氧化物 |
| C.此反应不属于复分解反应 |
| D.铝锅不宜长时间盛放碱性食品 |