(10分)请回答下列问题:
(1)等温、等容下,已知2NO+O2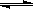 2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是 (填字母)。
2NO2 △H<0,当该反应处于平衡状态时,下列措施中有利于提高NO的平衡转化率的是 (填字母)。
| A.升高温度 | B.降低温度 | C.加入O2 | D.减小压强 |
E.加入催化剂 F.增加NO的量
(2)若将l.00 molO2和2.00 mol NO混合充入容积为2 L的密闭容器中,3分钟后反应达到平衡。平衡后混合气体总物质的量为2.55mol,用O2表示的化学反应速率为 mol•L-1•min-1。
(3)容积均为2 L的四个密闭容器中均进行着(2)中的反应,某温度下,各物质物质的量(mol)及正逆反应速率关系如下表所示:
| 容器编号 |
n(O2) |
n(NO) |
n (NO2) |
v正与v逆的关系 |
| Ⅰ |
0.20 |
0.10 |
0.20 |
v正=v逆 |
| Ⅱ |
0.20 |
0.40 |
1.00 |
②v正___v逆? |
| Ⅲ |
0.60 |
1.20 |
0.80 |
③v正___v逆? |
①若方程式系数为最简整数比,则该温度下的平衡常数K=
填写表中空格: ② ③ (填>或 <)
(15分)有X、Y、Z三种元素,X是有机化合物中必含有的元素,Y是地壳里含量最高的元素,Z是质量最轻的元素,X与Y能结合成两种化合物A和B,A可以燃烧,B不可燃烧也不能支持燃烧,X与Z结合的化合物C是最简单的烃。由X、Y与Z三种元素组成的化合物D常用作实验室加热的燃料。
(1)试判断X、Y、Z各是什么元素(填名称)。X、Y、Z。
(2)试判断A、B、C、D各是什么物质(填化学式)。
A、B、C、D。
(3)写出化合物A与Fe2O3反应的化学方程式。
(4)已知常温下8g C在O2中完全燃烧放出444.8kJ的热量,试写出化合物C完全燃烧的热化学方程式:。
(5)欲用化合物D与Na反应制取并收集1g H2,需要D的质量g;并写出化合物D与 反应的化学方程式:。
反应的化学方程式:。
(10分) 请按要求填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的核组成符号:;
(2)CO2的电子式是,NH4Cl的电子式是;
(3)物质在下列变化过程中克服的是:①共价键②离子键。(填序号)
HCl溶于水;电解熔融NaCl制Na;电解水分解生成O2和H2。
(4)下列物质中:
互为同分异构体的有;互为同素异形体的有;
属于同位素的有;属于同一种物质的有。(填序号)
①液氯② ③白磷④氯气⑤
③白磷④氯气⑤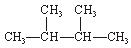
⑥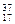 Cl⑦
Cl⑦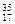 Cl⑧红磷
Cl⑧红磷
(4分)在水溶液中,短周期元素Y形成的YO3n-与S2-能发生如下离子反应:
YO3n-+3S2-+6H+Y-+3S↓+3H2O请回答:
(1)此反应中,氧化剂是_____________。(2)YO3n-中n= _______。
(3)Y元素在周期表中位于周期族。
(12分)
(1)乙烯通入溴的四氯化碳溶液中,观察到的现象是 ;其反应方程式为 ;乙烯在一定条件下发生加聚反应的化学方程式为 。
(2)苯分子的结构简式为。苯能发生取代反应,请任写一个苯发生取代反应的化学方程式
(3)把卷成螺旋状的铜丝在酒精灯外焰上加热,使表面变黑,然后迅速伸到无水酒精中,有什么现象,写出总反应的化学方程式,铜丝在反应中起的作用。
在一定条件下进行下列化学反应,请根据以下的转化关系回答下列问题,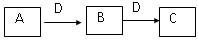
已知A、B、C中均含有同一种元素,D为非金属单质,能使带有火星的木条复燃。
(1)若A在常温下为气体,C是红棕色气体。
①写出A单质的电子式。
②C与水反应所得的溶液呈酸性,此反应中氧化剂与还原剂物质的量之比为
(2)若A为固体单质,C为淡黄色固体,,则C含有的化学键有,
A与水反应的离子方程式为。
(3)若A为日常生活中最常见的烃的衍生物,则A与C反应生成一种有水果香味的物质,其反应的化学方程式为,反应类型为反应。