在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)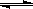 Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是
Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是
| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动 |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.达到化学平衡状态时,若c(CO)="0.100" mol/L,则c(CO2)="0.0263" mol/L |
据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是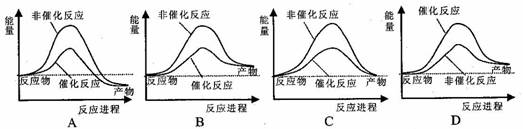
一定体积的密闭容器中进行如下反应:X2(g)+Y2(g) 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应充分进行后,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应充分进行后,各物质的浓度有可能是
| A.Z为0.3mol/L | B.Y2为0.4mol/L | C.X2为0.2mol/L | D.Z为0.4mol/L |
将4 mol A和2 mol B放入2 L密闭容器中发生反应2A(g) + B(g) 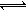 2C(g) ΔH<0。4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
2C(g) ΔH<0。4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
A.当c(A)︰c(B)︰c(C)=2︰1︰2时,该反应即达到平衡状态
B.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
C.达到平衡状态后,若只升高温度,则C的物质的量浓度增大
D.4 s内,v(B)=0.075 mol/(L ·s)
在容积可变的密闭容器中,2mo1N2和8mo1H2在一定条件下发生反应,达到平衡时,H2的转化率为25%,则平衡时的氮气的体积分数接近于
| A.5% | B.10% | C.15% | D.20% |
下列事实不能用勒夏特列原理解释的是
A.工业制取金属钾:Na(l)+ KCl(l) NaCl(l)+ K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来 NaCl(l)+ K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来 |
| B.冰镇啤酒瓶,把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。 |
| C.在实验室可用排饱和食盐水的方法收集氯气。 |
D.对于2HI(g) H2(g)+I2(g);ΔH>0,缩小容器的体积可使颜色变深。 H2(g)+I2(g);ΔH>0,缩小容器的体积可使颜色变深。 |