Al、Fe、Cu都是重要的金属元素。下列说法正确的是
| A.三者对应的氧化物均为碱性氧化物 |
| B.三者的单质放置在空气中均只生成氧化物 |
| C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D.电解AlCl3、FeCl3、CuCl2的混合溶液是阴极上依次析出Cu、Fe、Al |
某有机物的结构简式为: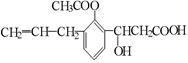 ,则此有机物可发生的反应类型有:①取代②加成③消去④酯化⑤水解⑥氧化⑦加聚⑧中和 ( )
,则此有机物可发生的反应类型有:①取代②加成③消去④酯化⑤水解⑥氧化⑦加聚⑧中和 ( )
| A.①②④⑤⑥⑦⑧ | B.②③④⑤⑥⑧ |
| C.②③④⑤⑥⑦⑧ | D.①②③④⑤⑥⑦⑧ |
从松树中分离得到的松柏醇,其结构简式为,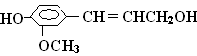
它既不溶于水,也不溶于碳酸氢钠溶液,能够跟1mol该化合物起反应的H2或Br2的最大用量分别是()
| A.1 mol,2 mol | B.4 mol,2 mol |
| C.4 mol,4 mol | D.4 mol,1 mol |
有甲酸甲酯、丙酸、乙酸乙酯的混合物7.4g,完全燃烧后,将所得气体通过碱石灰干燥管,充分吸收后干燥管增重18.6g,则混合物的平均相对分子质量为()
| A.69 | B.74 | C.77 | D.82 |
某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯四种物质中1种或几种,在鉴别时有下列现象:(1)有银镜反应;(2)加入新制Cu(OH)2悬浊液沉淀不溶解;(3)与含酚酞的NaOH溶液共热发现溶液中红色逐渐消失以至无色,下列叙述正确的有()
| A.几种物质都有 | B.有甲酸乙酯,可能有甲酸 |
| C.有甲酸乙酯和甲醇 | D.有甲酸乙酯,可能有甲醇 |
甲醛、乙酸和丙醛组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为()
| A.27% | B.28% | C.54% | D.无法计算 |