现有常见金属单质A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。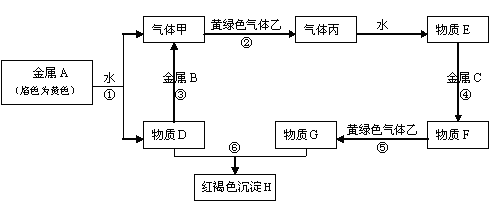
请根据以上信息回答下列问题:
⑴写出下列物质的化学式:
A B F 丙
⑵写出下列反应离子方程式:
反应③
反应⑤
反应⑥
(1)1.5molH2SO4的质量是________,其中含有______mol H,含有_______g氧元素。
(2)9.03×1023个氨分子含___________摩尔氨分子,____________摩尔氢原子,
____________摩尔质子,________________个电子。
(3)__________mol CO2中含有3g碳。标况下,_________L CO2中含有0.25mol 氧原子,____________mol CO2中含有3.01×1023个CO2分子,它的质量是______________。
A、B、C等八种物质有如下框图所示转化关系。又知,A是由地壳中含量最多的金属元素形成的单质,C、D、E是常见的由短周期元素形成的气体单质,气体F与气体G相遇产生大量的白烟,H是厨房中必备一种调味盐(部分反应物和生成物及溶剂水已略去)。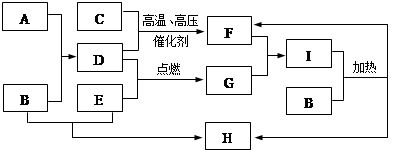
请回答下列问题:
⑴ B的化学式是,F的化学式是,H的电子式为;
⑵写出A和B溶液反应的离子方程式:; ⑶写出D和E反应的化学方程式:。
⑶写出D和E反应的化学方程式:。
⑷如何检验I中的阳离子。
①~⑤五种元素在元素周期表中的位置如下图所示:回答下列问题: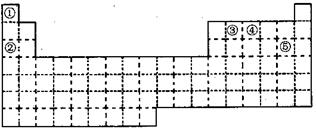
(1)①~⑤五种元素中,非金属性最强的元素在周期表中的位置是;
(2)②③④元素原子中,半径最小的是(填元素符号);
(3)元素①和③可以形成众成多的化合物,其中最简单的是(化学式)。该化合物中,化学键的类型为(选填“极性共价键”、 “非极性共价键”或“离子键”);
(4)元索④的最高价氧化物对应水化物能与其最低价的气态氢化物发生反应,产物是
(化学式);
(5)元素⑤单质与水反应的离子方程式:。
A、B、C、D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1) B元素的名称____,B在周期表中的位置第______周期,第________族;
(2) A、B形成的化合物的电子式____
(3) C的元素符号______,C的最高价氧化物的化学式____
(4) D的最高价氧化物对应的水化物的化学式____________
(1)元素最高正化合价为+6,其负化合价为____,某元素R与氢形成的气态氢化物的化学式为RH3,其最高价氧化物的化学式为___________
(2)下列各题中有关物质的比较,请用“>”、“<”、“=”填空
酸性: H3PO4HNO3,H2SO4HClO4
热稳定性:CH4NH3,HClHI
(3)1-18号元素中,最外层电子数是次外层电子数二倍的元素是,原子结构示意图,能与氧形成的氧化物的化学式、。