将Cl2制成漂白粉的最主要目的是:①使它转变成较易溶于水的物质 ②转变成较稳定、便于贮存的物质 ③提高氯的质量分数 ④提高漂白能力
| A.①②③ | B.②④ | C.②③ | D.② |
下列盛放试剂的方法正确的是 ( )
| A.氢氟酸或浓硝酸存放在带橡胶塞的棕色玻璃瓶中 |
| B.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中 |
| C.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中 |
| D.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
实验表明:将氯水滴加到一张蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中不正确的是
| A.此实验表明氯水具有酸性、漂白性 |
| B.内环呈白色外环呈红色或浅红 |
| C.内外环上颜色的差异表明此变化过程中,中和反应比氧化还原反应快 |
| D.氯水中形成次氯酸的反应中还原产物是HClO |
为提高农作物产量,改善农作物品质,有一种向温室内定期施放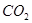 的方法是:将工业废稀
的方法是:将工业废稀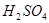 按1:4用水稀释后,盛放在塑料桶内悬挂于1.2米的高处,每天向桶内加入适量的某物质。下列物质中最适宜加入的是
按1:4用水稀释后,盛放在塑料桶内悬挂于1.2米的高处,每天向桶内加入适量的某物质。下列物质中最适宜加入的是
A. |
B. 粉末 粉末 |
C. 粉末 粉末 |
D. 粉末 粉末 |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物: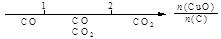 |
B.Fe在Cl2中的燃烧产物: |
C.AlCl3溶液中滴加NaOH后铝的存在形式: |
D.氨水与SO2反应后溶液中的铵盐: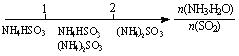 |
能正确表示下列反应的离子方程式为
| A.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH–= CO32-+ H2O |
| B.二氧化硫通入次氯酸钠溶液:SO2 + ClO- + 2OH–= SO42-+Cl-+ H2O |
| C.硫化钡加入稀硫酸:BaS + 2H+ = H2S↑+ Ba2+ |
| D.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O="3I" 2+6OH- |