在标准状况下,将40 mL NO和NO2的混和气体,与20 mL O2混合,跟水充分反应吸收后,还剩余6 mL无色气体,则原混合气体中NO2和NO分别是多少?(请写出计算过程)
工业上采用氨的催化氧化法制取硝酸。用10.0吨氨制取63%的硝酸,设NH3的转化率为95%,NO转化为HNO3的产率为90%,则实际能得63%硝酸的质量为多少吨?
常温下某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱溶液混合pH=7,求酸溶液体积V(酸)和碱溶液体积V(碱)的关系。
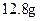 铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为
铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为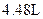 .
.  铜和硝酸反应的化学方程式为:
铜和硝酸反应的化学方程式为:

试计算:
(1)被还原的硝酸的物质的量
(2)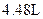 气体中各成分的物质的量
气体中各成分的物质的量
某工厂排出的废水,经测定含0.012mol·L-1的游离Br2和8×10-4mol·L-1的H+离子。若用加Na2SO3的方法除去Br2,化学反应为:Na2SO3+Br2+H2O—Na2SO4+HBr(方程式未配平),现处理这种废水5L,问①需加入0.05mol·L-1的Na2SO3溶液多少升才能把Br2除尽?②除尽后的废水中H+离子的物质的量浓度是多少?(溶液的体积变化忽略不计)
将3.2gCu溶于30mL amol/L过量的硝酸中,假设硝酸的还原产物只有NO和NO2,反应结束后,将所得溶液加水稀释至1000mL,测得c(NO3-)为0.2mol/L。求:
(1)稀释后溶液中氢离子的物质的量浓度为。
(2)生成的气体中NO的物质的量为,
NO2的物质的量为 (用含a的关系式表示)
(3)用NaOH溶液吸收氮的氧化物是防止NOx污染的一种方法。原理为:
2NO2+2NaOH="NaNO3+NaNO2+H2O;" NO2+NO+2NaOH=2NaNO2+H2O
若生成的混合气体能被NaOH溶液完全吸收,则a的取值范围为