下列各溶液中,c(Na+)最大的是
| A.0.8 L 0.4 mol/L的NaOH溶液 | B.0.2 L 0.15 mol/L的Na3PO4 |
| C.1 L 0.3 mol/L的NaCl溶液 | D.0.1 L 0.5 mol/L的NaCl溶液 |
A、B、C三种短周期元素在周期表中位置如下图所示,B位于ⅥA族.下列叙述错误的是()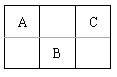
A.原子半径大小顺序为B>A>C
B.C的最高价氧化物的水化物酸性最强
C.BO2具有漂白性
D.A的氢化物水溶液呈碱性
下列说法不正确的是()
| A.化学反应是旧键断裂和新键形成的过程 |
| B.盖斯定律实质上是能量守恒定律的体现 |
| C.反应前后分子数发生改变的反应不遵循质量守恒定律 |
| D.溶解平衡、水解平衡和电离平衡均为动态平衡 |
化学与生产、生活、社会密切相关,下列有关说法中不正确的是()
| A.2009年10月1日,国庆60周年天安门广场庆祝晚会上燃放的“焰火”让全世界为之欢呼、倾倒,这主要是利用了化学中“焰色反应”的有关知识 |
| B.神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
| C.预防甲型HIN1流感的含氯环境消毒剂对人体无害 |
| D.第十一届全运会“东荷西柳”场馆使用的钢结构材料属于合金 |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是()
| A.含有碳碳双键、羟基、羰基、羧基 | B.含有苯环、羟基、羰基、羧基 |
| C.含有羟基、羰基、羧基、酯基 | D.含有碳碳双键、苯环、羟基、羰基 |
某有机化合物X,经过下列变化后可在一定条件下得到乙酸乙酯。则有机物X是()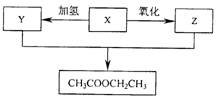
| A.C2H5OH | B. C2H4 | C.CH3CHO | D. CH3COOH |