在一密闭容器中进行下列反应: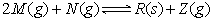 。在反应达到平衡后保持温度不变,若缩小容器的体积,则混合气体的平均相对分子质量( )
。在反应达到平衡后保持温度不变,若缩小容器的体积,则混合气体的平均相对分子质量( )
| A.一定增大 | B.一定减小 | C.一定不变 | D.不能确定 |
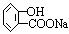
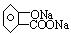
欲将转变为应选用的试剂为
| A.盐酸 | B.CO2 | C.NaOH | D.H2SO4 |
下列各组有机物,不论以何种比例混合,只要二者的物质的量之和不变,完全燃烧时所消耗的氧气的物质的量和生成的水的物质的量均分别相等的是
| A.甲烷和甲酸甲酯 | B.乙烷和乙醇 |
| C.苯和苯甲酸 | D.乙炔和苯 |
由饱和一元酸与饱和一元醇形成的酯同饱和一元醛组成的混合物共xg,测得其中含氧yg,则其中碳的质量分数为
| A.(x-y) | B.1-y/x | C.6/7(x-y) | D.6/7(1-y/x) |
下列实验能成功的是()
| A.苯与浓溴水反应(Fe作催化剂)制溴苯 |
| B.福尔马林与苯酚的混合物,沸水浴加热制酚醛树脂 |
| C.氯乙烯加聚的生成物能使酸性KMnO4溶液褪色 |
| D.加热硫酸、乙醇、氯化钠固体的混合物制氯乙烷 |
把有机物的混合物在一定条件下反应:①甲醇,乙醇和浓硫酸加热得到醚②乙二醇与乙酸酯化得酯③氨基乙酸与丙氨酸生成二肽,④苯酚和浓溴水,反应所生成的有机物的种类由多到少的顺序是:
| A.④③②① | B.①②③④ | C.③①②④ | D.③②①④ |