25℃时,若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是( )
| A.生成了一种强酸弱碱盐 | B.弱酸溶液和强碱溶液反应 |
| C.强酸溶液和弱碱溶液反应 | D.一元强酸溶液和一元强碱溶液反应 |
下列反应中,属于取代反应的是()
A.CH4 + 2 O2 CO2 + 2H2O CO2 + 2H2O |
B.CH2=CH2 + H2 CH3-CH3 CH3-CH3 |
C. + Br2 + Br2   + HBr + HBr |
D.2CH3CH2OH + O2 2CH3CHO + 2H2O 2CH3CHO + 2H2O |
鉴别葡萄糖和淀粉溶液可选用()
| A.AgNO3溶液 | B.石蕊试液 |
| C.稀硫酸 | D.含NaOH的Cu(OH)2悬浊液 |
CO和H2在一定条件下可以合成乙醇:2CO(g) + 4H2(g) 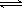 CH3CH2OH(g)+ H2O(g)
CH3CH2OH(g)+ H2O(g)
下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1:2的物质的量之比反应生成乙醇 |
| D.反应体系中乙醇的物质的量浓度不再变化 |
某有机物在空气中充分燃烧,生成的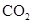 和
和 的物质的量之比为1:1,由此可以得出该有机物( )
的物质的量之比为1:1,由此可以得出该有机物( )
A.分子中C、H、O的个数比为1:2:3 B.分子中C和H的个数比为1:2
C.分子中肯定不含氧原子 D.分子中肯定含有氧原子
下图为铜锌原电池示意图,按该装置进行实验下列说法正确的是( )
| A.锌片逐渐溶解 |
| B.烧杯中溶液逐渐呈蓝色 |
| C.电子由铜片通过导线流向锌片 |
| D.该装置能将电能转变为化学能 |