下列各组离子在溶液中一定能大量共存的是 ( )
| A.PH=0的溶液:K+、Ca2+、HCO3-、NO3- |
| B. c(H+水)=1×10-10 mol/L溶液中:K+、Fe2+、SO42-、NO3- |
| C.使紫色石蕊变蓝的溶液:K+、Na+、CH3COO-、SO42- |
| D.存在较多的Na+、SO42-、OH-的溶液中:Mg2+、Ba2+、Br- |
在恒温恒容的容器中进行反应H2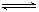 2H,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为
2H,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为
| A.等于18s | B.等于12s | C.大于18s | D.小于18s |
可逆反应2NO2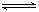 2NO + O2在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO + O2在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态
| A.①③ | B.②③④ | C.②③ | D.①④ |
下述实验设计合理的是
| A.用锌粒和稀硝酸反应制备H2 |
| B.用NH4NO3加热制取NH3 |
| C.大理石与稀硫酸反应制备CO2 |
| D.用焰色反应鉴别固体NaCl和 KCl |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2 + O2 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法不正确的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法不正确的是
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.化工生产中,可通过改变温度、浓度、压强等因素,提高SO2的转化率 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
在四个不同容器中,不同条件下进行合成氨反应。根据在相同时间内测定的结果判断生成氨的速率最快的是
| A.V(NH3)=0.5 mol•L-1•min-1 | B.V(H2)=0.3 mol•L-1•min-1 |
| C.V(N2)=0.2 mol•L-1•min-1 | D.V(H2)=0.01 mol•L-1• s -1 |