已知2H2(g) + O2(g) = 2H2O(l) ΔH =" -" 571.6 kJ/mol
H2O(l) = H2O(g) ΔH =" +" 44 kJ/mol 下列说法中,不正确的是
| A.H2的燃烧热为285.8 kJ/mol |
| B.2H2(g) + O2(g) = 2H2O(g)ΔH =" -" 483.6 kJ/mol |
| C.1 mol H2完全燃烧生成气态水放出的热量大于285.8 kJ |
| D.形成1 mol H2O的化学键释放的总能量大于断裂1 mol H2和0.5 mol O2的化学键所吸收的总能量 |
丁腈橡胶具有许多优良性能,结构简式为 ,合成丁腈橡胶的原料是( )
,合成丁腈橡胶的原料是( )
①CH2=CH—CH=CH2②CH3—C≡C—CH3③CH2=CH—CN
④CH3—CH ="CH" - CN⑤CH3—CH=CH2⑥CH3—CH=CH—CH3
| A.③⑥ | B.②③ | C.①③ | D.④⑤ |
在下列反应中,不可能在有机物中引入羧基的是 ( )
| A.一卤代烃的水解 | B.酯在酸性条件下水解 |
| C.醛的氧化 | D.烯烃的氧化 |
某种解热镇痛药的结构简式为下图: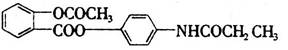 ,当它完全水解时,可得到的产物有( )
,当它完全水解时,可得到的产物有( ) 
| A.2种 | B.3种 | C.4种 | D.5种 |
下列关于蛋白质的叙述中,不正确的是 ( )
| A.向蛋白质溶液里加(NH4)2SO4溶液可提纯蛋白质 |
| B.在豆浆中加入少量的石膏,能使豆浆凝结为豆腐 |
| C.温度越高,酶对某些化学反应的催化效率越高 |
| D.当人误食重金属盐类时,可以喝大量的牛奶、蛋清解毒 |
实验室区别下列物质选用的试剂(括号中的为试剂,必要时可加热)不正确的是( )
| A.苯和己烯(溴水) | B.矿物油和植物油(NaOH溶液) |
| C.淀粉和纤维素(碘水) | D.硝基苯和CCl4(水) |