在一定条件下,可逆反应A2(g)+B2(g)  2C(g)在一个密闭容器中达到平衡时,测得c(A2)=0.5mol•L-1, c(B2)=0.1mol•L-1,c(C)=1.6mol•L-1。若A2、B2、C的起始浓度分别为a mol•L-1、b mol•L-1、g mol•L-1请确定:
2C(g)在一个密闭容器中达到平衡时,测得c(A2)=0.5mol•L-1, c(B2)=0.1mol•L-1,c(C)=1.6mol•L-1。若A2、B2、C的起始浓度分别为a mol•L-1、b mol•L-1、g mol•L-1请确定:
(1)a、g应满足的关系式为_________。
(2)若反应从正反应方向开始进行,当g=_________,a有最大值为_________。
(3)若反应从逆反应方向开始进行,当b=_________,a有最小值为_________。
(4)b的取值范围为________________。
在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的氢气时,硫酸恰好用完,则:
(1)产生这些气体消耗的锌的质 量是多少?
(2)通过导线的电子的物质的量是多少?
(3)原稀硫酸的物质的量浓度是多少?
已知NaCl(s)+H2SO4(浓)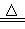 NaHSO4+HCl↑,现有117g NaCl和足量的浓硫酸完全反应。求:
NaHSO4+HCl↑,现有117g NaCl和足量的浓硫酸完全反应。求:
(1)产生的HCl在标况时的体积为多少?
(2)将所得HCl气体溶于100g水中,若所得盐酸的密度为1.1 g/mL,则盐酸的物质的量浓度为多少?
在一密闭容器中,用等物质的量的A和B发生如下反应:A(g)+2B(g) 2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,求这时A的转化率。
2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,求这时A的转化率。
将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下发生反应:
2SO2+ O2 2SO3达到平衡时,测得平衡混合物总的物质的量为5mol。
2SO3达到平衡时,测得平衡混合物总的物质的量为5mol。
求:(1)平衡时O2的物质的量浓度;
(2)平衡时SO2的转化率;
(3)平衡时SO3的体积分数。
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为L,NO2的体积为L。
(2)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为mol/L。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水
g。