农用化肥和城市生活污水排放会使地下水含氮量增高,其中对人体有害的含氮污染物的主要形态是( )。
| A.NH4+ | B.NO2- | C.NO3- | D.有机氮 |
现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4; ②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5。则下列有关比较中正确的是( )
| A.原子半径:④>③>②>① | B.第一电离能:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:①>④>③=② |
下列是几种原子的基态电子排布,电负性最大的原子是( )
| A.1s22s22p63s23p64s2 | B.1s22s22p63s23p3 |
| C.1s22s22p63s23p2 | D.1s22s22p4 |
下列表达式错误的是( )
A.甲烷的电子式: |
B.氮原子的L层电子排布图: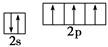 |
| C.硫离子的核外电子排布式:1s22s22p63s23p4 |
| D.碳12原子: 612C |
下列溶液中微粒的物质的量浓度关系正确的是( )
A.常温下0.1 mol/L的下列溶液① NH4Al(SO4)2、② NH4Cl、③ NH3·H2O、④ CH3COONH4溶液中,c(NH )由大到小的顺序是②>①>④>③ )由大到小的顺序是②>①>④>③ |
| B.常温下0.4 mol/L CH3COOH溶液和0.2 mol/L NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度大小顺序为: c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C.0.1 mol/L Na2CO3溶液与0.1 mol/L NaHCO3溶液等体积混合: c(CO  )+2c(OH-)=c(HCO )+2c(OH-)=c(HCO )+3c(H2CO3)+2c(H+) )+3c(H2CO3)+2c(H+) |
D.0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(NH )+c(NH3·H2O)=2c(SO )+c(NH3·H2O)=2c(SO ) ) |
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。下列叙述正确的是( ) 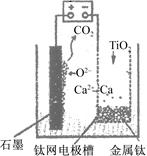
| A.该电池工作过程中O2-向阴极移动 |
| B.阳极的电极反应式为C+2O2--4e-===CO2↑ |
| C.若用铅蓄电池作该装置的供电电源,“-”接线柱应连接PbO2电极 |
| D.在制备金属钛前后,整套装置中CaO的总量减少 |