(10分)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)  xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于________________
(2)A的转化率为_________________
(3)生成D的反应速率为_________________
(4)如果增大反应体系的压强,则平衡体系中C的质量分数_________(填变大、变小、不变)
(5)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各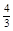 mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入________物质_________mol
mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入________物质_________mol
(共12分)写出下列反应的化学方程式
(1)乙烯的水化
(2)丙烯的加聚反应
(3)苯的溴代
(4)甲苯的硝化
(5)二丙醇的氧化反应
(6)乙烯的实验室制取原理
(1)写出下列微粒的电子式:
①CH 3- ②-OH ③C 2H 2 ④OH -
(2)命名 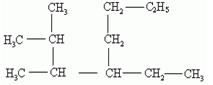
(用数字序号填空,共 9分)有①NH2-CH2-COOH②CH2OH(CHOH)4CHO③(C6H10O5)n(纤维素)④HCOOC2H5⑤苯酚⑥HCHO等物质,其中:
9分)有①NH2-CH2-COOH②CH2OH(CHOH)4CHO③(C6H10O5)n(纤维素)④HCOOC2H5⑤苯酚⑥HCHO等物质,其中:
(1)难溶于水的是,易溶于水的是,常温下在水中溶解度不大,70℃时可与水任意比例互溶的是。
(2)能发生银镜反应的是。
(3)能发生酯化反应的是。
(4)能跟氢气发生加成反应的是,能在一定条件下跟水反应的是。
(5)能跟盐酸反应的是,能跟氢氧化钠溶液反应的是。
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是________ ;
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是;
③、④、⑦氢化物稳定性由强到弱的顺序是;
(3)③与⑤按原子个数1:1所成的化合物的电子式为________________;该化合物与水反应的离子方程式为_______________。
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为__________ _;
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱:。
一定温度下在10L容器中加入5molSO2和3molO2,当反应达到平衡时,有3molSO2发生了反应,则:
(1)生成了_________molSO3,SO2的转化率为_________(用百分数表示)。
(2)平衡时容器内气体的总物质的量为_________。
(3)平衡时SO2的浓度是_________ ,O2的浓度是_________,SO3的浓度是_________ 。