草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:
称取Wg草酸晶体,配成100.00mL无色水溶液。量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定。试回答:
(1)滴定时所发生反应的化学方程式为
(2)草酸是二元弱酸,则草酸的电离方程式为 请从“电离平衡”的角度解释:为什么草酸的第二步电离比第一步难
(3)实验中不需要的仪器有(填序号)___________,还缺少的仪器有(填名称)______________________________。
a.托盘天平(带砝码,镊子) b.酸式滴定管 c.碱式滴定管 d.100mL容量瓶 e.烧杯
f.漏斗 g.锥形瓶 h.玻璃棒 i.药匙 j.烧瓶
图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是___________mL。图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_____________。
| A.是amL | B.是(25-a)mL | C.一定大于amL | D.一定大于(25-a)mL |
(4)实验中,标准液KMnO4溶液应装在_______式滴定管中。若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值会_____(偏大、偏小、无影响)达到滴定终点,溶液由 色变为 色;
(5)在滴定过程中若用amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_____________mol·L-1;
(6)若测得x=2,称取某二水合草酸晶体0.1200 g,加适量水完全溶解,然后用0.02000 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 。
现有A、B、C、D、E、X、Y和M等物质,它们均为纯净物,在一定条件下可发生下列转化: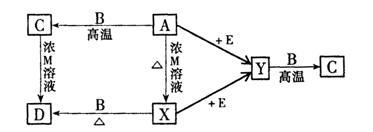
其中:X、Y为常见双原子气体单质(X为有色气体);B为常见金属单质,质软;C
溶于强酸和强碱;E为由两种常见元素(按原子个数l︰1)组成的液体;A为黑色化合物。上述各步转化中只写出其中一种生成物,其它生成物没有写出(也有可能反应只有一种生成物)。试回答:
(1)写出化学式:X , E 。
(2)写出离子反应方程式:
A→X:;C→D:。
(3)X+E反应的化学方程式为。
过氧化钠保存不当容易变质。
(1)某过氧化钠样品已经部分变质,请你设计实验,限用一种溶液,证明过氧化钠已经变质。
(2)检验样品中还有过氧化钠的方法是。
(3)某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设
计用下图装置来测定过氧化钠的质量分数。 上图中的E和F构成量气装置,用来测定O2的体积。
上图中的E和F构成量气装置,用来测定O2的体积。
①写出装置A和B中发生反应的离子方程式:
装置A:,装置B:。
②NaOH的作用是。
③本实验中测量气体体积时应注意的事项有
。
④他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为VmL,则样品
中过氧化钠的质量分数为。
下图表示在没有通风橱的条件下制备氯气时设计的装置, 图中a、
b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)
⑴仪器A的名称是;
水槽中应盛放的是;
烧杯中盛放的是;
烧瓶中反应的化学方程式;
⑵在收集氯气时,应打开,关闭__。
当氯气收集完毕时打开,关闭__ _。(填a,b)
⑶ 若要制得标准状况下的Cl20.672L,理论上需要MnO2的物质的量是多少?
某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:
(1)甲装置的名称是____________ (填“原电池”或“电解池”)。
(2) 写出电极反应式: pt极______ ______;
当甲中产生0.1 mol气体时,乙中析出铜的质量应为___________________;
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色___________(填“变深”、“变浅”或“无变化”)。
(Ⅱ)由Cu2+、Cl-、Na+、SO42-四种离子中的两种离子组成的电解质溶液若干种,可选用铜电极、铂电极进行电解实验。
(1)要使电解过程中溶质的组成和质量不变,而该稀溶液的浓度增大,又无浑浊,应以______为阳极电解________溶液,阳极电极反应式为_________________________________。
(2)以铂作阳极电解 ________ 溶液时,溶液的碱性有明显增强,且溶液保澄清,电解的总反应式为 ________________________________________。
Zn—MnO2干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
(1)该电池的负极材料是。电池工作时,电子流向(填“正极”或“负极”)。
(2)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
。欲除去Cu2+,最好选用下列试剂中的(填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是。若电解电路中通过2mol电子,MnO2的理论产量为克。