某厂生产的产品碳酸钠中混有少量碳酸氢钠。为了测定产品中碳酸钠的质量分数,取100g样品加热(2NaHCO3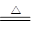 Na2CO3 + H2O + CO2↑ ,碳酸钠受热不分解),完全分解生成二氧化碳气体0.22g。求:
Na2CO3 + H2O + CO2↑ ,碳酸钠受热不分解),完全分解生成二氧化碳气体0.22g。求:
(1)样品中碳酸氢钠的质量。
(2)样品中碳酸钠的质量分数。
把10g铁和铜的混合物放到盛有足量盐酸的烧杯中,充分反应后,烧杯中物质的总质量比反应前(铁、铜混合物和盐酸)减少了0.2g,求原混合物中铜的质量分数.
某铁合金样品1.1g在氧气完全燃烧得到0.013g二氧化碳,通过计算确定该铁合金是生铁还是钢?
实验中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。
请根据以上信息计算:样品中碳酸钙的质量分数?
同学们已经学习了氧气和二氧化碳的实验室制法,请你参与总结与分析:
【仪器认识】装置A中仪器的名称:a(1),b(2);装置C的名称:(3)
【反应原理】用双氧水和二氧化锰混合制取氧气的化学方程式为(4);
用大理石和稀盐酸制取二氧化碳的化学方程式为(5)。
【制取装置】用氯酸钾与二氧化锰制取氧气,可选用的发生装置是(6),若收集较纯净的氧气最好选用(7)装置,收满的现象是(8)。
实验室制取二氧化碳气体,可选用的装置组合是(9)或(10),
检验二氧化碳是否收满的方法是(11)(简述实验操作、现象、结论)。
比较B、C装置,C装置在制取气体时,明显的优点是(12)。
【数据分析】实验小组用氯酸钾和二氧化锰的混合物制取氧气,反应过程中混合物的质量变化如图所示。完全反应后最终收集到0.3 mol氧气。
①请根据化学方程式列式计算原混合物中含氯酸钾的质量。(13)
②图中P点处试管内的固体物质有(14)
为测得某大理石样品中碳酸钙的质量分数,兴趣小组同学进行了如下实验,过程如图所示:(杂质不溶于水也不与盐酸反应)
求:①反应中生成二氧化碳的物质的量为 (15)mol
②该大理石样品中碳酸钙的质量分数(16)。(根据化学方程式计算)