一定条件下,在容积为10L的密闭容器中,1molX和1molY进行如下反应:2X(g)+Y(g) Z(g)经60s达到平衡,生成0.3molZ,下列说法正确的是
Z(g)经60s达到平衡,生成0.3molZ,下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001mol/(L·s) |
B.将容器容积变为20L,Z的平衡浓度为原来的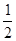 |
| C.若增大压强,则正反应速率增大,逆反应速率减小 |
| D.若升高温度,X的体积分数增大,则该反应的△H<0 |
在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比6:1:2,则溶液中Na2SO4、NaCl、NaOH个数比为()
| A.1:1:1 | B.1:4:2 | C.1:2:4 | D.1:3:2 |
将等物质的量浓度、等体积的硫酸与烧碱溶液混合后,滴入紫色石蕊试液,溶液呈( )
| A.紫色 | B.红色 | C.蓝色 | D.无色 |
设NA代表阿伏加德罗常数,下列说法正确的是()
| A.23g金属钠变为钠离子时得到的电子数为NA |
| B.标准状况下,18g水所含的电子数目为9NA |
| C.标准状况下,11.2L氦气所含的原子数目为NA |
| D.标准状况下,2.24 LN2和O2的混合气体所含原子数为0.1NA |
下列有关实验用品的使用或操作的叙述中,正确的是()
| A.用红色石蕊试纸检验溶液的酸性 |
| B.容量瓶用于配制准确浓度的溶液,但不能作为反应容器使用 |
| C.配制稀硫酸时,先向烧杯中注入浓硫酸,再加水稀释 |
| D.称量NaOH固体时,将NaOH直接用手拿放在托盘上的纸上 |
实验室进行Na2SO4溶液蒸发时,一般有下列操作过程,其正确的操作顺序为:①固定铁圈位置 ②停止加热,余热蒸干 ③放置酒精灯 ④放蒸发皿 ⑤加热搅拌
| A.①③④⑤② | B.③①④⑤② |
| C.①④③⑤② | D.③④①⑤② |