下列各项中,电离方程式正确的是
A.HCO3-+H2O CO32-+ H3O + CO32-+ H3O + |
B.H2SO3=2H++SO32- |
C.NaHCO3 Na++HCO3- Na++HCO3- |
D.NaHSO4(熔融)=Na++H++ SO42- |
下列离子方程式书写正确的是
| A.硫酸铝与氨水反应:Al3++3OH-=Al(OH)3 ↓ |
| B.碳酸钙溶于醋酸:CaCO3+2H+ =Ca2++H2O+CO2 ↑ |
| C.氯气跟水反应:Cl2 + H2O = 2H++ Cl-+ClO- |
| D.NaHCO3溶液中加入盐酸:H++HCO3-= CO2↑+H2O |
下列图示的四种实验操作名称从左到右依次是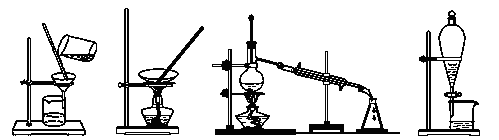
| A.蒸发、蒸馏、过滤、萃取 | B.过滤、蒸馏、蒸发、萃取 |
| C.过滤、蒸发、蒸馏、分液 | D.萃取、蒸馏、蒸发、过滤 |
足量的两份铝粉分别与等体积的盐酸和NaOH 溶液反应,同温同压下产生的气体体积比为1:1,则盐酸和NaOH溶液的物质的量浓度之比为
| A.2:3 | B.3:1 | C.1:2 | D.1:1 |
能证明SO2具有漂白性的是
| A.品红溶液中通入SO2气体,溶液红色消失 |
| B.溴水中通入SO2气体后,溶液褪色 |
| C.滴入酚酞的NaOH溶液中通入SO2气体,红色消失 |
| D.酸性KMnO4溶液中通入SO2气体后,溶液褪色 |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA |
| B.22.4L SO2含有NA个SO2分子 |
| C.1.6g CH4所含的电子数为NA |
| D.标况下,4.48L的水中含有H2O分子的数目为0.2NA |