常温下,下列溶液中的微粒浓度关系正确的是
| A.新制氯水中加入固体NaOH:c(Na+) = c(Cl−) + c(ClO−) + c(OH−) |
| B.pH = 8.3的NaHCO3溶液:c(Na+) > c(HCO3−) > c(CO32−) > c(H2CO3) |
| C.pH = 11的氨水与pH = 3的盐酸等体积混合:c(Cl−) = c(NH4+) > c(OH−) = c(H+) |
| D.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合: |
2c(H+) – 2c(OH−) = c(CH3COO−) – c(CH3COOH)
下列四个试管中,过氧化氢分解产生氧气的反应速率最慢的是

下列物质中,既有离子键,又有共价键的是
| A.KCl | B.NH4Cl | C.H2O | D.CH4 |
下列化学用语错误的是
A.NaCl的电子式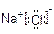 |
B.甲烷的结构式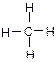 |
C.Mg原子结构示意图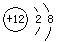 |
D.乙烯的结构简式CH2=CH2 |
S和S2—两种粒子中,不相同的是
①核内质子数②核外电子数③最外层电子数④核外电子层数
| A.①② | B.②③ | C.③④ | D.②③④ |
X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物为强碱,Z 的原子半径最小。据此判断下列说法不正确的是
| A.X是第ⅠA元素,Z是第ⅦA元素 |
| B.X、Y、Z三种元素的最高化合价依次升高 |
| C.Z的最高价氧化物对应的水化物是强酸 |
| D.如果Y的最高价氧化物的水化物难溶于水,则Y一定是Al |