将等物质的量的A、B混合于2L的密闭容器中,发生下列反应3A(g)+B(g) xC(g)+2D(g),经反应5min后,测知D的浓度为0.5mol/L,A、B的物质的量浓度之比为3∶5,C的平均反应速率是0.1mol/(L·min),试计算:
xC(g)+2D(g),经反应5min后,测知D的浓度为0.5mol/L,A、B的物质的量浓度之比为3∶5,C的平均反应速率是0.1mol/(L·min),试计算:
(1)x的值?
(2)5min内B的平均反应速率?
(3)5min时A的物质的量浓度?
将一定量铜与足量浓硝酸充分反应,可以得到6.72L NO2气体(气体体积在标准状况下测定)。
(1)写出铜与浓硝酸反应化学方程式。标明电子转移的方向和数目。
(2)若反应后溶液体积为100mL,则所得溶液中Cu2+的物质的量浓度是多少?
(3)若改用排水法收集气体,则可收集到气体的体积为多少?
纳豆是一种减肥食品,从其中分离出一种由C、H、O三种元素组成的有机物A,为确定其结构现进行如下各实验:
① 6.0g物质A在一定条件下完全分解,生成3.36L(标准状况)一氧化碳和1.8g水。
②中和0.24g物质A,消耗0.2mol/L的氢氧化钠溶液20.00mL。
③ 0.01mol物质A完全转化为酯,需乙醇0.92g;0.01molA能与足量钠反应放出0.336L标准状况下的氢气。
试确定(1)A的摩尔质量和化学式(2)A的结构简式
(6分)用足量的NaOH溶液将448mlCl2(标准状况)完全吸收,计算①生成的NaClO的物质的量;②该反应中氧化剂与还原剂的物质的量之比;③该反应中电子转移总数。
(4分)用1L水吸收246.4L(标准状况)氯化氢气体,得到密度为1.15g.cm-3的盐酸,计算:(1)该盐酸溶液的物质的量浓度;(2)该盐酸溶液中氯化氢的质量分数。
实验室里用二氧化锰与浓盐酸反应 来制取适量的氯气。现用浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为11.2升,(假设HCl全部参加反应)
来制取适量的氯气。现用浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为11.2升,(假设HCl全部参加反应)
(M
 nO2+4HCl(浓)
nO2+4HCl(浓)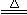 MnCl2+2H2O+Cl2↑)
MnCl2+2H2O+Cl2↑)
计算:(1)参加的二氧化锰的质量。(2)被氧化的HCl的物质的量。