25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是( )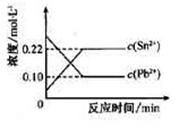
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
设NA为阿伏加德罗常数,下列叙述正确的是
| A.27 g铝原子最外层电子数为2NA |
| B.2. 4g镁与足量盐酸反应转移的电子数为0.1NA |
| C.1 molH2O分子所含电子数为10NA |
| D.标准状况下,22.4 L乙醇的分子数为NA |
下列常用实验仪器中,不能直接用于混合物的分离或提纯的是
| A.分液漏斗 | B.蒸发皿 | C.蒸馏烧瓶 | D.容量瓶 |
配制100 mL 0.10 mol·L-1的NaOH溶液时,下列实验操作会使所配溶液浓度偏大的是
| A.转移溶液时有液体飞溅 |
| B.在容量瓶中定容时俯视刻度线 |
| C.定容时凹液面最底处高于刻度线 |
| D.转移溶液后未洗涤烧杯就直接定容 |
下列实验操作或方法,不正确的是
| A.用蒸馏的方法制取蒸馏水 |
| B.用酒精萃取饱和碘水中的碘单质 |
| C.使用分液漏斗分离水和四氯化碳的混合物 |
| D.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
将饱和氯化铁溶液分别滴入下列液体中,能形成胶体的是
| A.冷水 | B.氯化钠溶液 | C.沸水 | D.氢氧化钠溶液 |