下列各图所示的气密性检查中,装置漏气的是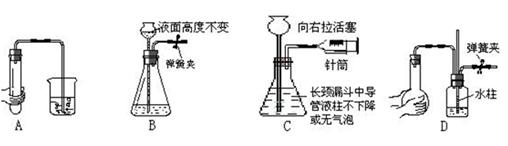
在理论上可用于设计原电池的化学反应是()
| A.2Al(s)+2NaOH(aq)+2H2O(1) = 2NaAlO2(ag)+3H2(g)△H <0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s)= BaCl2(aq)+2NH3·H2O(aq)+8H2O(l) △H >0 |
| C.CaC2(s)+2H2O(1) = Ca(OH)2(s)+C2H2(g)△H <0 |
| D.HCl(aq)+NaOH(aq) = NaCl(aq) + 3H2O(l)△H <0 |
下图中a、b、c、d、e为周期表前4周期的一部分,下列叙述正确的是()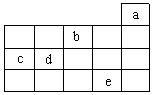
| A.b元素除0价外,只有一种化合价 |
| B.五种元素中,c元素形成的单质性质最稳定 |
| C.c、d元素最高价氧化物的水化物酸性:c > d |
| D.e元素在自然界中主要存在于海水中 |
下列说法正确的是()
| A.由H形成1 mol H-H键要吸收热量 |
| B.所有燃烧反应都是放热反应 |
| C.16g O3单质中含有的分子个数为NA |
| D.凡经加热而发生的化学反应都是吸热反应 |
有a、b、c、d四种元素。a、b的阳离子与c、d的阴离子具有相同的电子层结构;a的阳离子的正电荷数小于b的阳离子的正电荷数,c的阴离子的负电荷数大于d的阴离子的负电荷数。则它们的离子半径的关系是()
| A.a>b>c>d | B.c>d>a>b | C.c>a>d>b | D.b>a>d>c |
下列关于物质性质变化的比较,不正确的是()
| A.酸性强弱: HI > HBr > HCl > HF | B.原子半径大小: Na > S > O |
| C.碱性强弱: KOH > NaOH > LiOH | D.还原性强弱: F- > Cl- > I- |