某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,取该矿样为原料生产CuC12·2H2O 晶体。
已知:常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
| 金属离子 |
氢氧化物开始沉淀的pH |
氢氧化物沉淀完全的pH |
| Fe2+ |
7.0 |
9.0 |
| Fe3+ |
1.9 |
3.2 |
| Cu2+ |
4.7 |
6.7 |
回答下列问题:
(l)步骤①的焙烧过程中需要通入氧气。在实验室中,可使用常见化学物质利用上图所示装置制取氧气,试写出熟悉的符合上述条件的两个化学方程式:______________________、______________________。
(2)焙烧产生的尾气中含有的一种气体是形成酸雨的污染物,若将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:____________________、__________________。
(3)步骤②酸浸过程中,需要用到3 mol · L-1的盐酸100 mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有_______________________________________。
(4)步骤④加入物质X的目的是_________________________________________,物质X 可以选用下列物质中的______________________。
(A)氢氧化钠 (B)稀盐酸 (C)氨水 (D)氧化铜
(5)当溶液中金属离子浓度低于1×10-5 mol · L-1时,认为该金属离子沉淀完全,则Ksp[Fe(OH)2]=_____。
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为____________,
在X极附近观察到的现象是 :______________________;
Y电极上的电极反应式是_________________________,
检验该电极反应产 物的方法是:_______________________________。
物的方法是:_______________________________。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是_________,电极反应式是________________________。
(15分)
分别由C、H、O三种元素组成的有机物A、B、C互为同分异构体,它们分子中C、H、O元素的质量比为15︰2︰8,其中化合物A的质谱图如下。
A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1︰1︰2,它能够发生银镜反应。B为五元环酯。C的红外光谱表明其分子中 存在甲基。其它物质的转化关系如下:
存在甲基。其它物质的转化关系如下:
⑴A的分子式是:。A分 子中的官能团名称是:。
子中的官能团名称是:。
⑵B和G的结构简式分别是:、。
⑶写出下列反应方程式(有机物用结构简式表示)
D→C;
H→G。
⑷写出由单体F分别发生加聚反应生成的产物和发生缩聚反应生成的产物的结构简式:、。
(15分)
X、Y、W、M、N五种元素分别位于周期表中三个紧邻的周期,且原子序数逐渐增大,X和Y的氢化物都比同族元素氢化物的沸点高,但在同周期中却不是最高的。W是同周期元素中离子半径最小的元素。M原子的最外能层上有两个运动状态不同的电子。N是一种“明星金属”,广泛应用于航天、军事等工业领域。请回答下列问题:
⑴X、Y两种元素的元素符号是:、。X、Y可以形成一种共价化合物,其中两种元素最外层电子数都达到8,则其分子的空间构型是:;中心原子的杂化方式是:。
⑵X的氢化物易溶于水的其原因是:。
⑶N的电子排布式是:。
⑷X和Y两元素的第一电离能大小关系:小于(填元素符号)。
⑸M与Y形成的化合物的晶体类型属于:;其晶胞如图所示,其中M离子的配位数是:。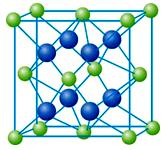
(15分)
纯碱一直以来都是工业生产的重要原料,很长一段时间来纯碱的制法都被欧美国家所垄断。上个世纪初我国著名的工业化学家侯德榜先生,经过数年的反复研究终于发明了优于欧美制碱技术的联合制碱法(又称侯氏制碱法)。并在天津建造了我国独立研发的第一家制碱厂。其制碱原理的流程如下:
⑴侯德榜选择天津作为制碱厂的厂址有何便利条件(举二例说明)、。
⑵合成氨工厂需要向制碱厂提供两种原料气体,它们分别是:、。(填化学式)这两种气体在使用过程中是否需要考虑添加的顺序:(填“是”或“否”),原因是:。
⑶在沉淀池中发生的反应的化学方程式是:。
⑷使原料水中溶质的利用率从70%提高到90%以上,主要是设计了(填上述流程中的编号)的循环。从母液中可以提取的副产品的应用是(举一例)。
(12分) 天然气(主要成分甲烷)是一种清洁、高效的能源,现在许多城市家庭用于厨房使用的燃料已经由煤气(主要成分是H2和CO按体积比1︰1混合的气体混合物)换成了天然气;此外天然气也是很好的燃料电池的燃料,甲烷在燃料电池中的能量转换率可达到85%—90%。请回答下列问题:
⑴已知H2、CO和CH4的燃烧热分别是286kJ/mol、283 kJ/mol和890 kJ/mol,则反应2CH4(g)+3O2(g)=CO(g)+H2(g)+CO2(g)+3H2O(l)的反应热△H=。
⑵以甲烷、空气为反应物,KOH溶液作电解质溶液构成燃料电池,则负极反应式为:。随着反应的不断进行溶液的pH(填“增大”“减小”或“不变”)。
⑶如果以该燃料电池为电源、石墨作两极电解饱和食盐水,则该电解过程中阳极反应式为:;如果电解一段时间后NaCl溶液的体积为1L,溶液的pH为12,则理论上消耗甲烷在标准状况下的体积为:mL。
⑷将⑶中电解结束后的溶液取出,向其中加入含有Mg2+和Fe2+的溶液甲,Mg(OH)2和Fe(OH)2同时生成,已知Mg(OH)2和Fe(OH)2在该温度下的溶度积常数分别是2×10—11和8×10—16,则甲溶液中Mg2+和Fe2+的浓度比为:。