已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是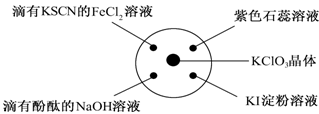
| 选项 |
实验现象 |
结论 |
| A |
滴有KSCN的FeCl2溶液变红 |
Cl2具有还原性 |
| B |
滴有酚酞的NaOH溶液褪色 |
Cl2具有酸性 |
| C |
石蕊溶液先变红后褪色 |
Cl2具有漂白性 |
| D |
KI-淀粉溶液变蓝 |
Cl2具有氧化性 |
下列说法不正确的是
| A.明矾、漂白粉、臭氧的净水原理相同 |
| B.“血液透析”的原理利用了胶体的性质 |
| C.食品包装中常放入有硅胶和铁粉的小袋,防止食物受潮和氧化变质 |
| D.煤炭燃烧、机动车尾气、建筑扬尘等可加重雾霾 |
下列各溶液中能大量共存的离子组是
| A.c(H+)=10-14 mol·L-1的溶液中:Na+、AlO2-、S2-、SO32- |
| B.使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C.碳酸氢钠溶液中:K+、SO42-、Cl-、H+ |
| D.使酚酞试液呈红色的溶液中:Mg2+、Cu2+、SO42-、K+ |
能正确表示下列反应的离子方程式为
| A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C.少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+H2SO3 |
| D.大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑ +H2O |
对于反应14CuSO4+5FeS2+12H2O===7Cu2S+5FeSO4+12H2SO4,下列说法正确的是
| A.只有硫酸铜作氧化剂 |
| B.SO42-既不是氧化产物又不是还原产物 |
| C.被氧化的硫与被还原的硫的质量比为3∶7 |
D.1 mol硫酸铜可以氧化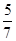 mol的硫 mol的硫 |
用草酸的稀溶液或草酸钠的酸性溶液可以洗涤粘在皮肤上的高锰酸钾,其离子方程式为(未配平):MnO4-+C2O42-+H+ CO2↑+Mn2++___。关于此反应的叙述正确的是
CO2↑+Mn2++___。关于此反应的叙述正确的是
| A.该反应右边方框内的产物是OH- |
| B.配平该反应后,H+的化学计量数是8 |
| C.该反应中氧化产物是CO2 |
| D.该反应电子转移总数是5e- |