硝酸亚铁溶液中存在主要平衡关系:Fe2++2H2O
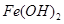 +2H+,若加入HCl则溶液的主要变化是( )
+2H+,若加入HCl则溶液的主要变化是( )
| A.变黄 | B.绿色变浅 | C.绿色加深 | D.无明显变化 |
下列说法正确的是
| A.酸碱中和反应是吸热反应 |
| B.吸热反应不加热就不会发生 |
| C.放热反应不用加热也一定能发生 |
| D.反应是放热还是吸热可以看反应物和生成物所具有的总能量的相对大小 |
“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10-9m,其研究成果广泛应用于催化及军事科学中,“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是
| A.溶液的性质 | B.胶体的性质 | C.浊液的性质 | D.无法确定 |
上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于
| A.无机物 | B.有机物 | C.盐类 | D.非金属单质 |
已知同一碳原子连有两个羟基不稳定: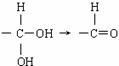 。有机物
。有机物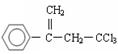 是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快。下列有关该有机物的说法不正确的是
是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快。下列有关该有机物的说法不正确的是
| A.属于卤代烃,能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色 |
| B.该物质既有手性异构,也有顺反异构 |
| C.在碱性条件下充分水解,可生成羧酸盐 |
| D.1mol 该物质在一定条件下可与4molH2发生加成反应 |
一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量是
| A.1.4g | B.2.2g | C.4.4g | D.在2.2g和4.4g之间 |