用1 000 g溶剂中所含溶质的物质的量来表示的溶液浓度叫做质量物质的量浓度,其单位是mol·kg-1。5 mol·kg-1的硫酸的密度是1.289 4 g·cm-3,则其物质的量浓度是( )
| A.3.56 mol·L-1 | B.5.23 mol·L-1 | C.4.33 mol·L-1 | D.5.00 mol·L-1 |
现有四种元素的基态原子的电子排布式如下:
①l s2 2s2 2p6 3s2 3p4②l s2 2s2 2p6 3s2 3p3③1s2 2s2 2p3④1 s2 2s2 2p5
则下列有关比较中正确的是 ( )
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>③=②>① |
A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中第一电离能最大。下列有关叙述错误的是 ( )
A四种元素A、B、C、D分别为O、Ca、Na、Ar
B.元素A、B、C两两组成的化合物可为CaO、Ca02、Na2 0、 Na2 02等
C元素A、C简单离子的半径大小关系为A<C
D-元素A、C电负性大小关系为A>C
下列说法正确的是()
| A.含n molHCl的浓盐酸与足量MnO2反应可生成n NA /4 个氯分子() |
B.在密闭容器中建立了N2+3H2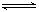 2NH3的平衡,每有17gNH3生成,必有0.5NA个NH3分子分解 2NH3的平衡,每有17gNH3生成,必有0.5NA个NH3分子分解 |
| C.同温同压同体积的CO2和SO2所含氧原子数均为2NA |
| D.20 g重水(D2O)中含有的电子数为10NA |
NA代表阿伏加德罗常数,下列说法正确的是()
| A.12.4g白磷含有的P—P键数目为0.4NA |
| B.15.6gNa2O2与过量的CO2反应时,转移的电子数为0.4NA |
| C.标准状况下,a L甲烷和乙烷混合气体中的分子数为a NA /22.4 |
| D.5.6 g铁粉与硝酸完全反应失去的电子数一定为0.3NA |
足量锌投入到1L14mol/L浓硫酸中充分反应,经测定没有硫酸剩余则此过程转移的电子数()
| A.大于14NA | B.等于14NA | C.小于14NA | D.无法确定 |