下列关于反应能量的说法正确的是
| A.101kPa时,2H2(g)+O2(g)=2H2O(l) ΔH="-571.6" kJ·mol-1,H2的燃烧热为571.6 kJ·mol-1 |
| B.Zn(s)+CuSO4(aq)=ZnSO4 (aq)+Cu(s) ΔH="-216" kJ·mol-1,反应物总能量>生成物总能量 |
| C.H+(aq)+OH-(aq)=H2O ΔH="-57.3" kJ·mol-1,含1molNaOH的氢氧化钠的溶液与含0.5molH2SO4的浓硫酸混合后放出57.3kJ的热量 |
| D.相同条件下,如果1molH所具有的能量为E1,1molH2所具有的能量为E2,则2 E1= E2 |
为使以面粉为原料的面包松软可口,通常用碳酸氢钠作发泡剂,因为它()
①热稳定性差 ②增加甜味 ③产生二氧化碳 ④提供钠离子
| A.②③ | B.①③ | C.①④ | D.③④ |
下列物质露置在空气中,质量会减轻的是()
| A.NaOH | B.浓H2SO4 | C.Na2O2 | D.Na2CO3·10H2O |
在一定温度下,向足量的饱和Na2CO3溶液中加入1.06 g无水Na2CO3,搅拌后静置,最终所得晶体的质量( )
| A.等于1.06 g | B.大于1.06 g,而小于2.86 g |
| C.等于2.86 g | D.大于2.86 g |
下列各组物质中的两物质作用时,反应条件或反应物用量的改变,对生成物没有影响的是( )
| A.Na2O2和CO2 | B.Na和O2 | C.NaOH和CO2 | D.C和O2 |
用1 L 1.0 mol·L-1 NaOH溶液吸收0.8 mol CO2,所得溶液中的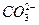 和
和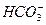 的物质的量浓度之比约是( )
的物质的量浓度之比约是( )
| A.1∶3 | B.1∶2 | C.2∶3 | D.3∶2 |