有下列三个氧化还原反应:
① 2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2 ;
②2FeCl2 + Cl2 = 2FeCl3;
③ 2KMnO4 + 16HCl =" 2KCl" + 2MnCl2 + 5Cl2↑+ 8H2O。
若某溶液中有Fe2+、I-、Cl-共存,要除去I-而不使Fe2+和Cl-的量减少,可加入的试剂是
| A.Cl2 | B.KMnO4 | C.FeCl3 | D.HCl |
随着科技的飞速发展,出现了许多新型无机材料,如植入生物体内的生物陶瓷材料HAP[化学式为Cam(PO4)n(OH)2],已被医疗上用于修补人的骨骼和牙组织,HAP的化学式中m等于( )
A. |
B. |
C.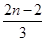 |
D.n+1 |
碳化硼(B4C)陶瓷硬度大,熔点高,具有化学惰性。据此判断,下列不能作为碳化硼陶瓷用途的是( )
A.作耐磨材料 B.作润滑材料 C.制切削工具 D.制钢化玻璃
复合材料是一类新型的、有前途的材料。目前,复合材料最主要的应用领域是( )
| A.高分子分离膜 | B.人工器官 | C.宇宙航空工业 | D.新型药物 |
将一定量的CO2缓慢地通入500ml NaOH溶液中,充分反应后将溶液低温蒸发,得到不含结晶水的白色固体A 9.50g。取3份质量不同的A,分别与100ml相同物质的量浓度的盐酸反应,得到的气体体积(标准状况)与A的质量关系如下表所示:()
| 组别 |
I |
II |
III |
| 盐酸体积/ml |
100 |
100 |
100 |
| A的质量/g |
1.90 |
3.42 |
3.80 |
| 气体的体积/ml |
448 |
716.8 |
672 |
下列说法不正确的是
A.第I组样品盐酸有剩余
B.若加入0.38g样品,则最终放出气体67.2mL
C.原NaOH的物质的量浓度是0.3mol·L—1
D.盐酸的物质的量浓度的0.5mol/L
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:()
2NH3(g)△H=一92.6kJ/mol.实验测得起始、平衡时的有关数据如下表:()
| 容器 |
起始各物质的物质的量/mol |
达平衡时体系能量的变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量:23.15kJ |
| ② |
0.6 |
1.8 |
0.8 |
Q(>0) |
下列叙述不正确的是( )
A.容器①、②中反应的平衡常数相等
B.容器②中达平衡时放出的热量Q
C.平衡时,两个容器中NH3物质的量浓度均为2mol/L
D.若容器①体积为0.2L,则平衡时放出的热量大于23.15kJ