在一密闭的容器中,反应aA(g)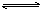 bB(g)达平衡后,保持温度不变,,当达到新的平衡时,B的浓度是原来的60%,则
bB(g)达平衡后,保持温度不变,,当达到新的平衡时,B的浓度是原来的60%,则
| A.平衡向正反应方向移动了 | B.物质A的转化率减少了 |
| C.物质B的质量分数增加了 | D.a > b |
200℃时,11.6 g CO2和水蒸气的混合气体与过量的Na2O2充分反应后,固体质量增加了3.6 g,再将反应后剩余固体冷却后加入含有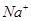 、
、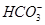 、
、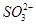 、
、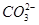 等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是 ( )
等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是 ( )
| A.原混合气体的平均摩尔质量为23.2 g/mol |
| B.混合气体与Na2O2反应过程中电子转移的物质的量为0.25 mol |
C.溶液中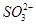 的物质的量浓度基本保持不变 的物质的量浓度基本保持不变 |
D.溶液中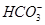 的物质的量浓度减小, 的物质的量浓度减小,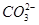 的物质的量浓度增大,但是 的物质的量浓度增大,但是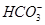 和 和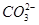 的物质的量浓度之和基本保持不变 的物质的量浓度之和基本保持不变 |
下列反应所得溶液中一定只含一种溶质的是( )
| A.向AlCl3溶液中加入过量NaOH溶液 |
| B.向NaOH溶液中通入CO2气体 |
| C.向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 |
| D.向NaHCO3溶液中加入CaC2固体 |
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑。下列说法中正确的是( )
| A.被氧化的元素与被还原的元素质量比为1︰4 |
| B.NaBH4既是氧化剂又是还原剂 |
| C.NaBH4是还原剂,H2O是氧化剂 |
| D.硼元素被氧化,氢元素被还原 |
将磁性氧化铁放入稀HNO3中可发生如下反应:
3Fe3O4+ 28HNO3=9Fe(NO3)x + NO↑+ 14H2O下列判断合理的是( )
| A.Fe(NO3)x中的x为2 |
| B.反应中每还原0.4 mol氧化剂,就有1.2 mol电子转移 |
| C.稀HNO3在反应中只表现氧化性 |
| D.磁性氧化铁中的所有铁元素全部被氧化 |
某溶液中含有SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的只有Na+
②有胶状物质生成
③有气体产生
④溶液颜色发生变化
⑤共发生了2个氧化还原反应
| A.①②③④⑤ | B.①②③④ | C.①③⑤ | D.②④⑤ |