根据所学知识,完成下列要求。
(1)0.2 mol OH-的质量为 ,其中含有 个电子;标况下 L HCl气体溶于水可配成12 mol/L HCl溶液500 mL。
(2)我国是最早使用铜及其合金的国家之一,我国古代劳动人民更最早利用天然铜的化合物进行湿法炼铜,这是湿法技术的起源,是世界化学史上的一项发明。西汉《淮南子·万毕术》记载:曾青得铁则化为铜,曾青为硫酸铜。
在该反应中被氧化的元素是 ,氧化剂是 ;该反应的离子方程式为: 。
(3)就有关物质的分离回答下面的问题。
①现有一瓶A和B的混合液,已知它们的性质如下表。
| 物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
溶解性 |
| A |
-11.5 |
198 |
1.11 |
A、B互溶,且均易溶于水 |
| B |
17.9 |
290 |
1.26 |
据此分析,将A和B相互分离的常用方法是 。
②在分液漏斗中用一种有机溶剂萃取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。
答: 。
已知25 ℃时部分弱电解质的电离平衡常数数据如表所示: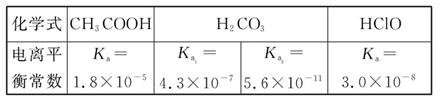
回答下列问题:
(1)物质的量浓度均为0.1 mol·L-1的四种溶液:
a.CH3COONab.Na2CO3c.NaClOd.NaHCO3
pH由小到大排列顺序是(用编号填写)。
(2)常温下,0.1 mol/L的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是。
| A.c(H+) |
| B.c(H+)/c(CH3COOH) |
| C.c(H+)·c(OH-) |
| D.c(OH-)/c(H+) |
E.c(H+)·c(CH3COO-)/c(CH3COOH)
(3)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是。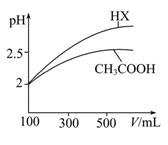
(1)将等质量的Zn粉分别投入:a:10 mL 0.1 mol·L-1 HCl和
b:10 mL 0.1 mol·L-1醋酸中。(填“>”、“=”或“<”)
①若Zn不足量,则反应速率ab,
②若Zn过量,产生H2的量ab。
(2)将等质量的Zn粉分别投入pH=1,体积均为10 mL的a:盐酸b:醋酸中
①若Zn不足量,则起始反应速率ab,
②若Zn过量,产生H2的量ab。
已知可逆反应:A(g)+B(g) C(g)+D(g)ΔH<0。请回答下列问题:
C(g)+D(g)ΔH<0。请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(A)="1" mol/L,c(B)="2.4" mol/L,达到平衡时,A的转化率为60%,此时B的转化率为。
(2)若反应温度降低,则B的转化率将(填“增大”、“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为c(A)="4" mol·L-1,c(B)=" a" mol·L-1,达到平衡后c(C)="2" mol·L-1,则a=。
(4)若反应温度不变,反应物的起始浓度分别为c(A)="c(B)=b" mol/L,达到平衡后c(D)=。(保留两位有效数字)
甲醇可通过将煤气化过程中生成的CO和H2在一定条件下,发生如下反应制得:CO(g)+2H2(g) CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题: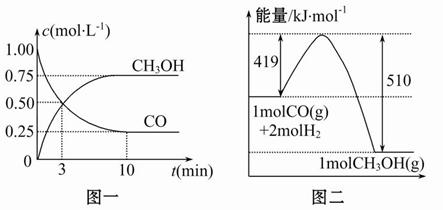
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=,CO的转化率为。
(2)该反应的平衡常数表达式为,温度升高,平衡常数(填“增大”、“减小”或“不变”)。
(3)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则加入各物质后该反应向(填“正”、“逆”)反应方向移动,理由是。
高炉炼铁中发生的基本反应之一为:FeO(s)+CO(g) Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
(1)该反应的平衡常数表达式为。
(2)温度升高,化学平衡移动后,平衡常数K值(填“增大”、“减小”或“不变”)。
(3)1 373 K时测得高炉中c(CO2)="0.025" mol/L,c(CO)="0.1" mol/L,在这种情况下,该反应是否处于化学平衡状态(填“是”或“否”)。此时,化学反应速率v(正)v(逆)(填“大于”、“等于”或“小于”),其原因是。