水的电离过程为H2O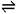 H++OH-,在不同温度下其平衡常数为:K(25℃)=1.0×10-14, K(35℃)=2.1×10-14,则下列叙述正确的是
H++OH-,在不同温度下其平衡常数为:K(25℃)=1.0×10-14, K(35℃)=2.1×10-14,则下列叙述正确的是
| A.c(H+)随温度的升高而降低 | B.在35℃时,c(H+)>c(OH-) |
| C.水的电离度α(25℃)>α(35℃) | D.水的电离是吸热的 |
将0.1mol/L醋酸溶液加水稀释,下列说法正确的是
| A.溶液中c(H+)和c(OH-)都减小 | B.溶液中c(H+)增大 |
| C.醋酸电离平衡向左移动 | D.溶液的pH增大 |
下列措施有利于反应N2 (g) + 3H2 (g)  2NH3 (g) △H = -92kJ·mol-1平衡向正反应方向移动的是
2NH3 (g) △H = -92kJ·mol-1平衡向正反应方向移动的是
①升高温度②降低温度③增大压强④减小压强⑤增大NH3浓度⑥减小NH3浓度
| A.②④⑥ | B.①③⑥ | C.②③⑤ | D.②③⑥ |
一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是()
| A.9.2g | B.10.6g | C.6.2g | D.4.6g |
24mL浓度为0.05mol/L的Na2SO3溶液恰好与15mL浓度0.02mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为()
| A.+2 | B.+3 | C.+4 | D.+5 |