下列实验“操作和现象”与“结论”对应关系正确的是
| |
操作和现象 |
结论 |
| A |
处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 |
Ksp:CaCO3<CaSO4 |
| B |
用石墨作电极电解MgSO4溶液,某电极附近有白色沉淀生成 |
该电极为阳极 |
| C |
向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 |
氧化性:Cu2+>Fe3+ |
| D |
向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 |
该溶液中一定含有Ag+ |
定容容器中反应:N2(g)+3H2(g) 2NH3(g),下列措施不能提高其反应速率的是()。
2NH3(g),下列措施不能提高其反应速率的是()。
| A.升高温度 | B.使用催化剂 |
| C.充入稀有气体,增大体系压强 | D.增加N2和H2的起始量 |
反应:4A(g)+5B(g)=4C(g)+6D(g)在不同条件下进行,用不同的物质表示其反应速率如下,
则此反应在不同条件下进行最快的是()。
A.v(A)=2 mol·L-1·min-1B.v(B)=3 mol·L-1·min-1
C.v(C)=1 mol·L-1·min-1D.v(D)=2.4 mol·L-1·min-1
某元素原子的质量数为A,它的阳离子Xn+核外有x个电子,w克这种元素的原子核内中子数为
A.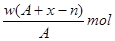 |
B.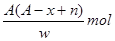 |
C.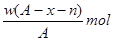 |
D.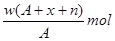 |
已知25 ℃、101 kPa下,下列反应
C(石墨) + O2(g) === CO2(g) ,燃烧1 mol C(石墨)放热393.51 kJ。
C(金刚石) + O2(g) === CO2(g),燃烧1 mol C(金刚石)放热395.41 kJ。
可以得出的结论是
| A.金刚石比石墨稳定 | B.1 mol石墨所具有的能量比1 mol金刚石低 |
| C.金刚石转变成石墨是物理变化 | D.石墨和金刚石都是碳的同位素 |
键能是指破坏(或形成)1mol化学键所吸收(或放出)的能量。现查得:H-H、Cl-Cl和H-Cl的键能分别为436KJ/mol、243KJ/mol和431KJ/mol,请用此数据估计,由Cl2、H2生成1molHCl时的热效应为
| A.放热91.5KJ | B.放热183KJ | C.吸热183KJ | D.吸热91.5KJ |