设NA表示阿伏加德罗常数,下列有关说法正确的是
| A.3.4g NH3中含N—H键数目为0.2 NA |
| B.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA |
| C.7.8 g Na2O2含有的阴离子数目为0.2 NA |
| D.46g NO2和N2O4的混合气体中含有的原子个数为3NA |
一定温度和电压下,电解精制食盐水可制取NaClO3。电解装置如图。已知:3Cl2 + 6OH- = ClO3-+ 5Cl-+ 3H2O。下列说法正确的是
| A.铁为阳极,电极反应式为2H2O + 2e- = H2↑+ 2OH- |
| B.若阴极产生3.36L(标况)气体,则溶液中的反应转移电子0.30mol |
C.电解槽内总反应方程式为:NaCl + 3H2O  NaClO3 + 3H2↑ NaClO3 + 3H2↑ |
| D.用阳离子交换膜代替阴离子交换膜,也一样可以制得NaClO3 |
实验室对茶叶中铁元素的检验,可经以下四个步骤完成:①将茶叶灼烧灰化;②茶叶灰用浓硝酸浸取并加蒸馏水稀释;③过滤得到滤液;④用KSCN溶液进行检验。下列说法中正确的是
| A.步骤①所用仪器包括蒸发皿、酒精灯、玻璃棒等 |
| B.步骤②所用的浓硝酸应保存在带橡皮塞的棕色试剂瓶中 |
| C.步骤③可以不做,改为将悬浊液静置一段时间 |
| D.步骤④观察到溶液变红色,证明茶叶中含有Fe3+ |
X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示,下列说法正确的是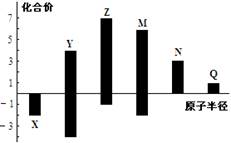
| A.金属性:N>Q |
| B.最高价氧化物对应水化物酸性:M>Y>N |
| C.简单离子半径:Q>N>X |
| D.原子序数:Z>M>Y>X |
下列措施,一定能使NaCl溶液中c(OH-)减小的是
| A.加热使c(H+)增大 | B.投入一小块金属钠 |
| C.加入少量NH4Cl固体 | D.以铁为电极进行电解 |
下列关于有机物的说法中,正确的是
| A.油脂和蛋白质都是天然高分子化合物,都能水解 |
| B.天然气和液化石油气的主要成分都是烃,都能燃烧 |
| C.苯和乙烯都含有碳碳双键,都能和H2发生加成反应 |
| D.裂化汽油和四氯化碳都不溶于水,都可用于萃取溴 |