氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO4溶液和“某物质”在40~50 ℃时反应可产生它。下列有关叙述中错误的是
| A.“某物质”具有还原性 |
| B.CuH与盐酸反应,可能产生H2 |
| C.CuH在氯气中燃烧:CuH+Cl2===CuCl+HCl |
| D.CuH与足量的稀硝酸反应:CuH+3H++NO3—===Cu2++NO↑+2H2O |
下列有关物质的性质或应用说法正确的是
| A.二氧化硫可用来加工食品,使食品增白 |
| B.SiO2既能溶于NaOH溶液又能溶于HF,说明SiO2是两性氧化物 |
| C.蛋白质水解生成葡萄糖放出热量,提供生命活动的能量 |
| D.锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
化学科学需要借助化学专业语言来描述,下列有关化学用语正确的是
A.含有10个中子的氧原子 |
B.NH4H的电子式: |
C.铝离子的结构示意图 |
D.甲烷分子的比例模型: |
“化学,我们的生活,我们的未来”是2011年“国际化学年”的主题。你认为下列行为中,不符合这一主题的是
| A.在家用燃煤中加入适量的生石灰能有效减少二氧化硫的排放量 |
| B.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 |
| C.开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料 |
| D.实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |
下列离子方程式正确的是
A.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+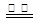 H2↑+ Cl2↑ H2↑+ Cl2↑ |
B.用银氨溶液检验乙醛中的醛基:CH3CHO +2Ag(NH3)2+ + 2OH-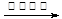 CH3COO- + NH4+ +3NH3 + 3Ag↓+ H2O CH3COO- + NH4+ +3NH3 + 3Ag↓+ H2O |
C.苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O- 2C6H5OH + 2CO32- 2C6H5OH + 2CO32- |
| D.为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 |
香兰素是重要的香料之一,它可由丁香酚经多步反应合成。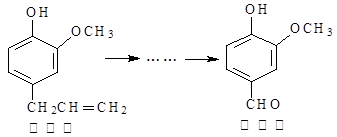
有关上述两种化合物的说法正确的是
| A.常温下,1 mol丁香酚只能与1 molBr2反应 |
| B.丁香酚不能FeCl3溶液发生显色反应 |
| C.1 mol香兰素最多能与3 mol氢气发生加成反应 |
| D.香兰素分子中至少有12个原子共平面 |